斯特鲁普测试对轻微性肝性脑病的诊断价值
DOI: 10.3969/j.issn.1001-5256.2022.04.017
-
摘要:
目的 探讨神经心理学测试——斯特鲁普(Stroop)测试对轻微性肝性脑病(MHE)的诊断价值。 方法 选取2020年8月-2021年3月于蚌埠医学院第一附属医院感染性疾病科住院治疗的96例肝硬化患者, 进行数字连接试验A(NCT-A)、数字符号试验(DST)、动物命名试验(ANT)及Stroop测试, 记录测试结果并收集临床数据。正态分布的计量资料组间比较采用t检验; 非正态分布的计量资料2组间比较采用Mann-Whitney U检验。计数资料组间比较采用χ2检验。采用ROC曲线评价Stroop测试对MHE的诊断价值, Pearson相关系数分析Stroop测试结果与NCT-A、DST、ANT的相关性。 结果 96例肝硬化患者中, MHE患病率为30.21%(29/96)。Stroop测试的Off+On总时间诊断MHE时的截断值为212.49 s, 其AUC为0.845, 敏感度为93.10%, 特异度为64.20%。Pearson相关系数分析结果显示, Stroop测试结果中的On+Off时长、On时长与NCT-A呈中等相关(r值分别为0.580、0.590, P值均 < 0.01), Off时长与NCT-A呈强相关(r=0.620, P < 0.01);On+Off时长、On时长、Off时长与DST均呈强相关(r值分别为-0.650、-0.650、0.630, P值均 < 0.01)。 结论 在诊断MHE中, Stroop测试是一项敏感度高、无需专业设备、结果易读、诊断价值高的方法。 Abstract:Objective To investigate the value of Stroop test, a neuropsychological test, in the diagnosis of minimal hepatic encephalopathy (MHE). Methods A total of 96 patients with liver cirrhosis who were hospitalized in Department of Infectious Diseases, The First Affiliated Hospital of Bengbu Medical College, from August 2020 to March 2021 were enrolled, and the number connection test-A (NCT-A), digit symbol test (DST), animal naming test (ANT), and Stroop test were performed for all patients. Test results were recorded and related clinical data were collected. The t-test was used for comparison of normally distributed continuous data between two groups, and the Mann-Whitney U test was used for comparison of non-normally distributed continuous data between two groups; the chi-square test was used for comparison of categorical data between groups. The receiver operating characteristic (ROC) curve was used to investigate the value of Stroop test in the diagnosis of MHE, and the Pearson correlation coefficient was used to analyze the correlation of the results of Stroop test with those of NCT-A, DST, and ANT. Results For the 96 patients with liver cirrhosis, the prevalence rate of MHE was 30.21% (29/96). The Off+On time of Stroop test had a cut-off value of 212.49 s in the diagnosis of MHE, with an area under the ROC curve of 0.845, a sensitivity of 93.10%, and a specificity of 64.20%. The Pearson correlation analysis showed that the On+Off time and On time of Stroop test were moderately correlated with NCT-A(r=0.580 and 0.590, both P < 0.01), the Off time of Stroop test was strongly correlated with NCT-A(r=0.620, P < 0.01), and the On+Off time, On time, and Off time of Stroop test were strongly correlated with DST(r=-0.650, -0.650, and -0.630, all P < 0.01). Conclusion In the diagnosis of MHE, Stroop test is a highly sensitive method with easy-to-read results and a high diagnostic value and does not require professional equipment. -
Key words:
- Hepatic Encephalopathy /
- Stroop Test /
- Diagnosis
-
表 1 MHE患者与无MHE患者一般资料比较
Table 1. Comparison of general data between patients with MHE and without MHE
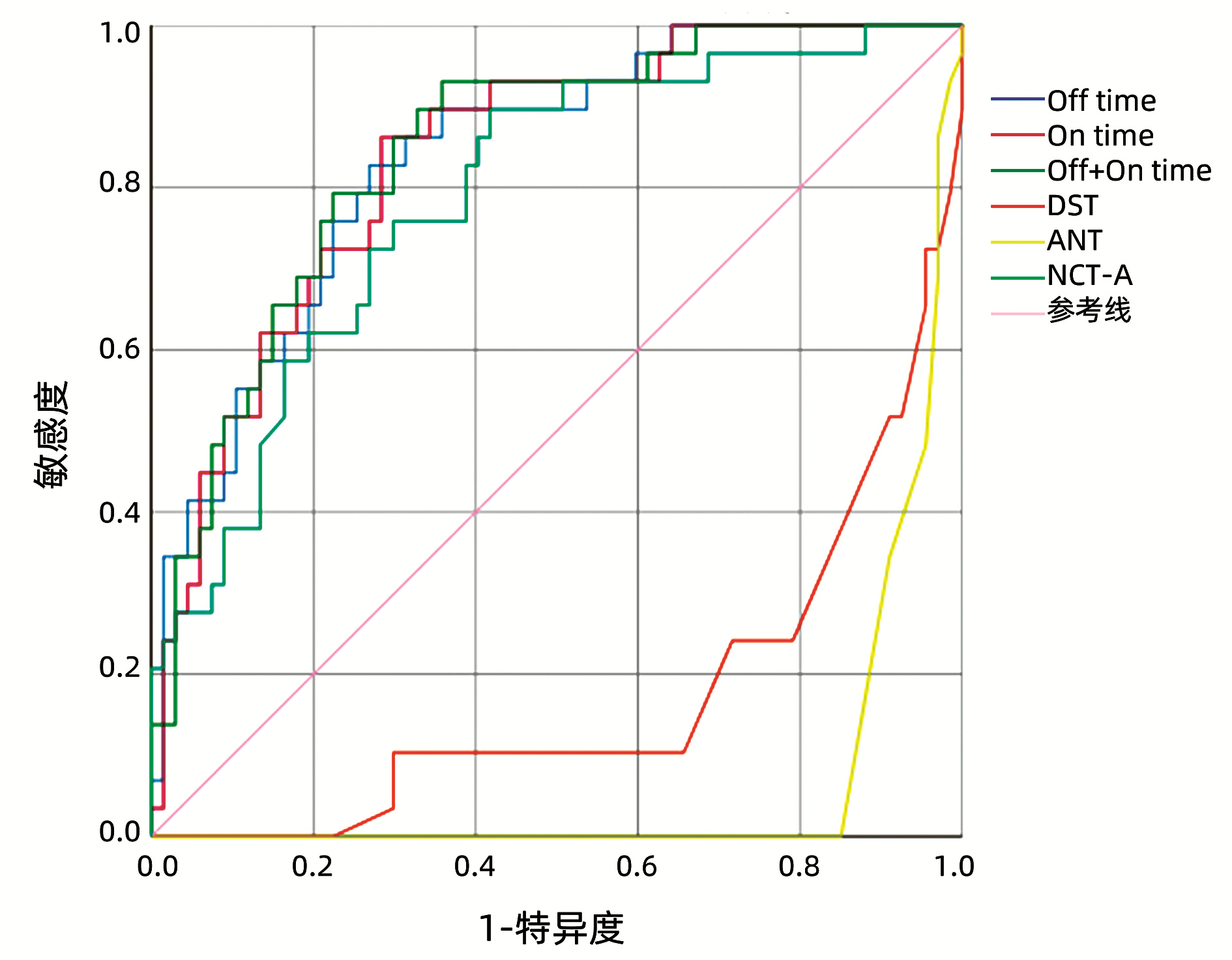
指标 MHE组(n=29) 无MHE组(n=67) 统计值 P值 年龄(岁) 52.07±7.91 46.34±9.30 t=2.891 0.005 WBC(×109/L) 3.75(2.50~5.28) 4.21(3.16~6.24) Z=-1.540 0.124 NEUT(×109/L) 2.20(1.41~2.78) 2.17(1.65~4.04) Z=-0.938 0.348 RBC(×1012/L) 3.64±0.87 3.90±0.79 t=-1.475 0.144 PLT(×109/L) 74.50(48.50~111.25) 95.00(56.00~153.00) Z=-1.313 0.189 PT(s) 14.40(12.58~17.88) 13.60(12.30~16.00) Z=-1.217 0.223 PTA(%) 68.18±19.60 74.17±18.74 t=-1.418 0.159 FIB(g/L) 2.08(1.61~2.46) 2.22(1.58~3.03) Z=-0.682 0.495 ALT(U/L) 29.00(19.25~55.00) 43.00(22.00~66.00) Z=-1.465 0.143 AST(U/L) 40.00(28.75~87.50) 59.00(38.00~114.00) Z=-1.751 0.080 ALP(U/L) 88.00(66.50~101.50) 110.00(77.00~160.00) Z=-2.326 0.020 TBil(μmol/L) 23.80(19.65~43.28) 25.60(14.60~49.70) Z=-0.539 0.590 Alb(g/L) 32.15±6.61 31.92±5.59 t=0.173 0.863 SCr(μmol/L) 64.00(50.25~71.00) 61.00(51.00~69.00) Z=-0.419 0.675 K+(mmol/L) 3.75±0.42 3.91±0.44 t=-1.639 0.105 CRP(mg/L) 3.40(1.93~17.13) 6.40(2.30~28.70) Z=-0.950 0.342 血浆氨 71.45±29.89 64.16±26.10 t=1.201 0.233 MELD评分 12.00(8.25~14.75) 10.00(8.00~14.00) Z=-0.789 0.430 表 2 Stroop测试、NCT-A、DST和ANT对MHE诊断的ROC曲线结果
Table 2. ROC curve results of Stroop test, NCT-A, DST and ANT for MHE diagnosis
指标 AUC 截断值 敏感度(%) 特异度(%) Off时长 0.837 110.62 s 82.80 73.10 On时长 0.837 107.42 s 82.80 70.10 Off+On时长 0.845 212.49 s 93.10 64.20 ANT 0.065 14.50个 0 14.90 NCT-A 0.788 58.61 s 89.70 58.20 DST 0.172 29.50分 10.30 34.30 -
[1] Chinese Society of Hepatology, Chinese Medical Association. Guidelines on the management of hepatic encephalopathy in cirrhosis[J]. J Clin Hepatol, 2018, 34(10): 2076-2089. DOI: 10.3969/j.issn.1001-5256.2018.10.007.中华医学会肝病学分会. 肝硬化肝性脑病诊疗指南[J]. 临床肝胆病杂志, 2018, 34(10): 2076-2089. DOI: 10.3969/j.issn.1001-5256.2018.10.007. [2] AGRAWAL S, UMAPATHY S, DHIMAN RK. Minimal hepatic encephalopathy impairs quality of life[J]. J Clin Exp Hepatol, 2015, 5(Suppl 1): S42-S48. DOI: 10.1016/j.jceh.2014.11.006. [3] Chinese Society of Hepatology, Chinese Medical Association. Chinese guidelines on the management of liver cirrhosis[J]. J Clin Hepatol, 2019, 35(11): 2408-2425. DOI: 10.3969/j.issn.1001-5256.2019.11.006.中华医学会肝病学分会. 肝硬化诊治指南[J]. 临床肝胆病杂志, 2019, 35(11): 2408-2425. DOI: 10.3969/j.issn.1001-5256.2019.11.006. [4] WANG YL, SHAO LC, YANG Z. Diagnostic value of number connection test for minimal hepatic encephalopathy and related factors of cirrhosis complicated with hepatic encephalopathy[J]. Clin J Med Offic, 2020, 48(12): 1424-1426, 1429. DOI: 10.16680/j.1671-3826.2020.12.11.王雨丽, 邵丽春, 杨卓. 数字连接试验对轻微肝性脑病诊断价值及肝硬化并发肝性脑病相关因素分析[J]. 临床军医杂志, 2020, 48(12): 1424-1426, 1429. DOI: 10.16680/j.1671-3826.2020.12.11. [5] CAMPAGNA F, MONTAGNESE S, RIDOLA L, et al. The animal naming test: An easy tool for the assessment of hepatic encephalopathy[J]. Hepatology, 2017, 66(1): 198-208. DOI: 10.1002/hep.29146. [6] BAJAJ JS, THACKER LR, HEUMAN DM, et al. The Stroop smartphone application is a short and valid method to screen for minimal hepatic encephalopathy[J]. Hepatology, 2013, 58(3): 1122-1132. DOI: 10.1002/hep.26309. [7] LABENZ C, BARON JS, TOENGES G, et al. Prospective evaluation of the impact of covert hepatic encephalopathy on quality of life and sleep in cirrhotic patients[J]. Aliment Pharmacol Ther, 2018, 48(3): 313-321. DOI: 10.1111/apt.14824. [8] SAN MARTÍN-VALENZUELA C, BORRAS-BARRACHINA A, GALLEGO JJ, et al. Motor and cognitive performance in patients with liver cirrhosis with minimal hepatic encephalopathy[J]. J Clin Med, 2020, 9(7): 2154. DOI: 10.3390/jcm9072154. [9] LABENZ C, ADARKWAH CC, WÖRNS MA, et al. Management of hepatic encephalopathy in Germany: A survey among physicians[J]. Z Gastroenterol, 2020, 58(1): 49-56. DOI: 10.1055/a-1010-6974. [10] WANG JY, ZHANG NP, CHI BR, et al. Prevalence of minimal hepatic encephalopathy and quality of life evaluations in hospitalized cirrhotic patients in China[J]. World J Gastroenterol, 2013, 19(30): 4984-4991. DOI: 10.3748/wjg.v19.i30.4984. [11] GIMÉNEZ-GARZÓ C, GARCÉS JJ, URIOS A, et al. The PHES battery does not detect all cirrhotic patients with early neurological deficits, which are different in different patients[J]. PLoS One, 2017, 12(2): e0171211. DOI: 10.1371/journal.pone.0171211. [12] BAJAJ JS, DUARTE-ROJO A, XIE JJ, et al. Minimal hepatic encephalopathy and mild cognitive impairment worsen quality of life in elderly patients with cirrhosis[J]. Clin Gastroenterol Hepatol, 2020, 18(13): 3008-3016. e2. DOI: 10.1016/j.cgh.2020.03.033. [13] ZENG X, ZHANG LY, LIU Q, et al. Combined scores from the encephalapp stroop test, number connection test B, and serial dotting test accurately identify patients with covert hepatic encephalopathy[J]. Clin Gastroenterol Hepatol, 2020, 18(7): 1618-1625. e7. DOI: 10.1016/j.cgh.2019.11.018. [14] LABENZ C, BEUL L, TOENGES G, et al. Validation of the simplified Animal Naming Test as primary screening tool for the diagnosis of covert hepatic encephalopathy[J]. Eur J Intern Med, 2019, 60: 96-100. DOI: 10.1016/j.ejim.2018.08.008. [15] QU Y, LI T, LIN C, et al. Animal naming test for the assessment of minimal hepatic encephalopathy in Asian cirrhotic populations[J]. Clin Res Hepatol Gastroenterol, 2021, 45(5): 101729. DOI: 10.1016/j.clinre.2021.101729. -




 PDF下载 ( 2164 KB)
PDF下载 ( 2164 KB)

 下载:
下载:


