超声造影联合剪切波弹性成像技术对肝脏良恶性肿瘤诊断价值的Meta分析
DOI: 10.12449/JCH240719
Value of contrast-enhanced ultrasound combined with shear wave elastography in the diagnosis of benign and malignant liver tumors: A Meta-analysis
-
摘要:
目的 研究超声造影(CEUS)联合剪切波弹性成像(SWE)对肝脏肿瘤的诊断价值。 方法 本研究根据PRISMA指南完成,PROSPERO注册号:CRD42023491288。检索PubMed、Embase、Cochrane Library、中国知网、维普、万方数据库关于CEUS联合SWE诊断肝脏肿瘤的文献,检索时限为2000年1月—2023年10月,经筛选共纳入12篇文献,包含1 328例患者。以QUADAS-2工具对纳入的文献进行质量评估。采用Stata 15.0软件计算合并灵敏度、特异度、阳性似然比、阴性似然比、诊断比值比及异质性,绘制综合受试者工作特征曲线(SROC)并计算曲线下面积(AUC)。 结果 纳入病例中,包含病灶1 457个,其中恶性病灶764个,良性病灶693个,阳性率为52.44%,阴性率为47.56%,计算得到合并灵敏度、特异度、阳性似然比、阴性似然比、诊断比值比分别为0.94(95%CI:0.91~0.96)、0.92(95%CI:0.87~0.95)、12.00(95%CI:7.40~19.40)、0.06(95%CI:0.04~0.10)、191(95%CI:87~417),异质性检验结果为Q=54.78,df=11.00,P<0.001,I2=79.92%,95%CI:69.18%~90.66%,AUC为0.98。 结论 CEUS联合SWE技术对于肝脏良恶性肿瘤具有较高的诊断价值,值得临床推广使用。 Abstract:Objective To investigate the value of contrast-enhanced ultrasound (CEUS) combined with shear wave elastography (SWE) in the diagnosis of liver tumors. Methods This study was conducted according to the PRISMA guideline, with a PROSPERO registration number of CRD42023491288. PubMed, Embase, the Cochrane Library, CNKI, VIP, and Wanfang Data were searched for articles on CEUS combined with SWE in the diagnosis of liver tumors published from January 2000 to October 2023, and a total of 12 articles were included, with 1 328 patients in total. The QUADAS-2 tool was used to assess the quality of the articles included. Stata 15.0 software was used to calculate pooled sensitivity, specificity, positive likelihood ratio, negative likelihood ratio, diagnostic odds ratio, and heterogeneity. The summary receiver operating characteristic (SROC) curve was plotted, and the area under the SROC curve (AUC) was calculated. Results There were 1 457 lesions for the patients included, among whom there were 764 malignant lesions and 693 benign lesions, with a positive rate of 52.44% and a negative rate of 47.56%. Calculations obtained a pooled sensitivity of 0.94 (95% confidence interval [CI]: 0.91 — 0.96), a specificity of 0.92 (95%CI: 0.87 — 0.95), a positive likelihood ratio of 12.00 (95%CI: 7.40 — 19.40), a negative likelihood ratio of 0.06 (95%CI: 0.04 — 0.10), and a diagnostic odds ratio of 191 (95%CI: 87 — 417). The tests for heterogeneity showed Q=54.78, df=11.00, P<0.001, and I2=79.92% (95%CI: 69.18% — 90.66%), with an AUC of 0.98. Conclusion CEUS combined with SWE has a relatively high diagnostic value for benign and malignant liver tumors and thus holds promise for clinical application. -
Key words:
- Ultrasonography /
- Shear-Wave Elastography /
- Liver Neoplasms /
- Meta-Analysis
-
我国肝癌发病率较高,早期准确识别肝脏恶性病变具有重要意义[1]。虽然CT、MRI等影像技术在诊断肝脏小病变时具有较高的准确性,但不能实时动态观察肿瘤特征,且经济成本较高[2]。组织病理学检查虽能准确诊断,但为有创检查,并发症较多,且不能评估病灶周围情况。
超声检查因其使用限制相对较少、价格低廉、安全无创等优势,广泛应用于肝脏良恶性肿瘤诊断,其中超声造影(contrast enhanced ultrasound,CEUS)和剪切波弹性成像(shear wave elastography,SWE)两大分支技术的兴起,极大地提高了超声诊断的准确性[3]。超声造影通过动态观察病灶血液供应状况以判断肝脏肿瘤良恶性,对早期诊断具有非常重要的意义,但需要实时动态观察。SWE通过测量剪切波速度定量反映病灶硬度,从而判断其性质,受观察者自身能力和经验的影响小。但是,相同性质的病灶,因发展阶段不同导致组织结构不同时,会干扰超声弹性成像的诊断[4-5]。
故而,将两种诊断技术联合,互为补充诊断肝脏良恶性肿瘤的研究逐渐增多,既往研究表明,CEUS及SWE对肝脏良恶性肿瘤的鉴别能力均高于常规超声,而二者联合使用诊断肝脏肿瘤的准确性更高于单独使用CEUS或SWE。本研究拟将两者联合诊断的文献进行Meta分析,以期为临床提供循证医学证据。
1. 资料与方法
1.1 规程与注册
本研究根据PRISMA指南[6]完成,PROSPERO注册号:CRD42023491288。
1.2 文献检索
检索英文数据库PubMed、Cochrane Library、Embase,检索策略为(“Contrast-enhanced ultrasound” OR “CEUS” OR “Shear Wave Elastography” OR “SWE” OR “Sonoelastography” OR “Elastosonography”) AND (“Liver Cancer” OR “Hepatocellular Cancer” OR “Hepatic Cancer” OR “Liver Tumor” OR “Hepatocellular Tumor” OR “Hepatic Tumor” OR “Liver Carcinoma” OR “Hepatocellular Carcinoma” OR “Hepatic Carcinoma” OR “Liver Nodule” OR “Hepatocellular Nodule” OR “Hepatic Nodule” OR “Liver Neoplasm” OR “Hepatocellular Neoplasm” OR “Hepatic Neoplasm” OR “Intrahepatic Cholangiocarcinoma” OR “Hepatoblastoma” OR “Liver Metastase” OR “Hepatic Hemangioma” OR “Hepatic Focal Nodular Hyperplasia” OR “Hepatic Angiomyolipoma” OR “Hepatic Cyst” OR “Liver Abscess”)。检索中文数据库中国知网、维普、万方数据库,检索策略为(超声造影OR剪切波弹性成像OR弹性成像)AND(肝肿物OR肝局灶性病变OR肝肿瘤OR肝占位OR肝脏病变OR肝结节OR肝癌OR肝细胞癌OR肝内胆管癌OR肝母细胞瘤OR肝转移癌OR肝血管瘤OR肝局灶性结节增生OR肝血管平滑肌脂肪瘤OR肝囊肿OR肝脓肿)。对纳入文献的参考文献、相似文献进行人工二次检索。检索文献发表时间为2000年1月—2023年10月。
1.3 文献的纳入排除标准
纳入标准:(1)目前已发表的中、英文文献;(2)文献中肝脏病灶的性质需涵盖多种类型的恶性与良性肿瘤;(3)研究对象为人类;(4)文献中有明确的金标准(病理、临床随访或影像学检查);(5)可直接或者间接得出四格表数据,即真阳性值、假阳性值、假阴性值、真阴性值。排除标准:(1)综述、荟萃分析、会议摘要以及个案分析;(2)文献为CEUS和SWE单独诊断肝脏良恶性肿瘤的研究。
1.4 数据提取
由两名研究者独立提取纳入文献的作者、发表年份、性别比例、金标准等信息,如果文献中没有直接提供灵敏度、特异度,则由两名研究者独立计算出灵敏度、特异度。当两名研究者存在意见分歧时,与第三名研究者协商后定论。
1.5 文献质量评价
采用RevMan5.3软件的诊断性实验质量评价标准(QUADAS-2)工具来评估纳入文献的质量[7],即评估每篇纳入文献的偏倚风险和适用性。
1.6 统计学方法
采用Stata 15.0软件进行统计学分析。
1.6.1 异质性检验
首先对纳入的研究进行异质性检验,根据I2值判定纳入的文献是否存在异质性以及异质性大小,若P>0.05、I2≤50%,表明各研究间异质性较低,采用固定效应模型进行Meta分析;若P≤0.05,I2>50%,表明各研究间存在显著异质性,采用随机效应模型进行Meta分析,并进行敏感性分析、亚组分析或者Meta回归分析寻找异质性来源[8]。同时采用双变量箱式图评估异质性,若研究落于双变量箱式图之外,提示研究存在异质性。
1.6.2 Meta分析
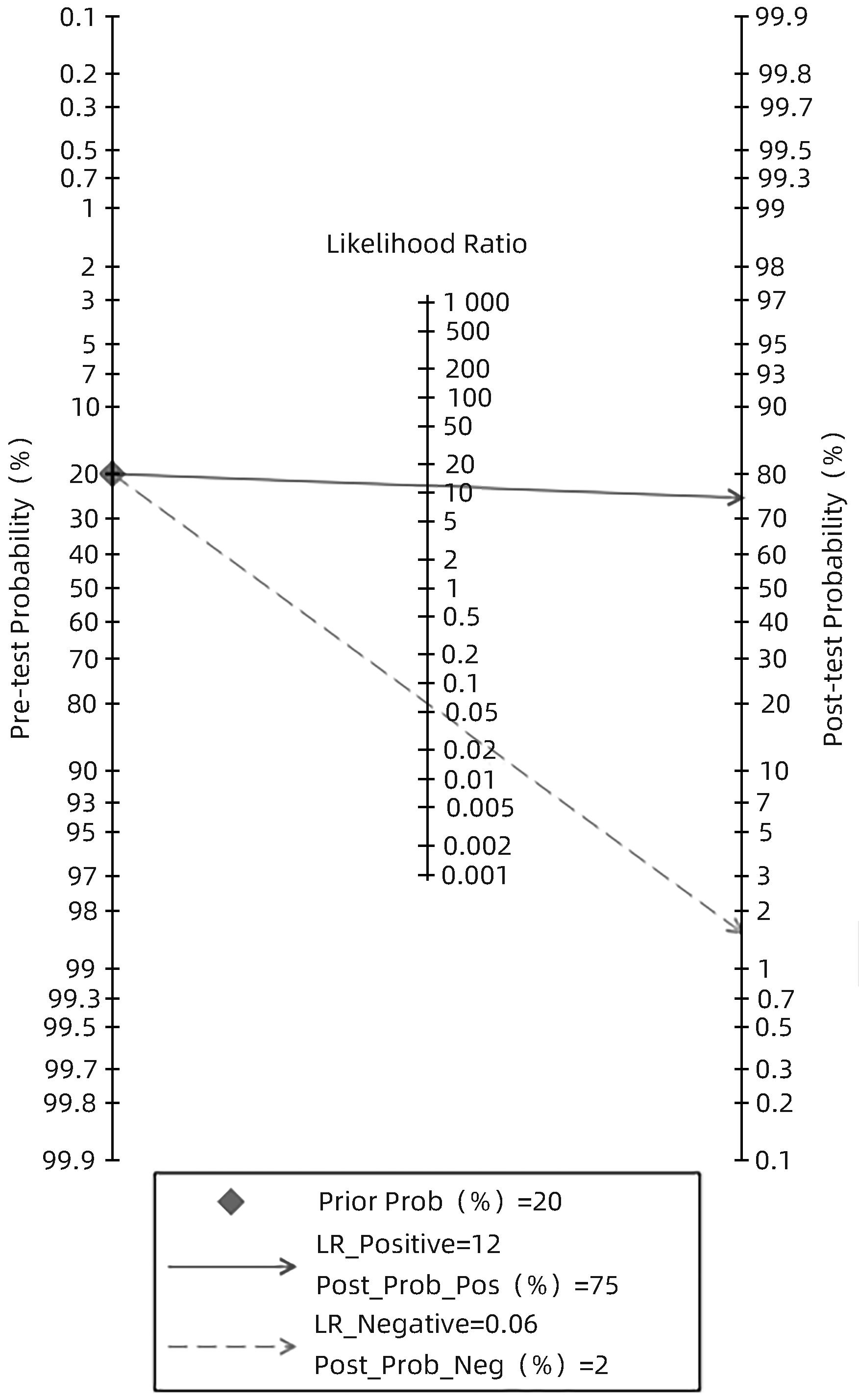
根据异质性大小选择相应的效应模型进行Meta分析,分别计算合并效应量和综合受试者工作特征曲线(SROC曲线)下面积(AUC),并进行敏感性分析评价本次研究结果的稳定性。用Fagan图显示验前概率(临床医生通过患者的病史、体征及个人经验评估的概率)及验后概率(诊断试验之后评估的患病概率)的关系。
1.6.3 发表偏倚分析
通过Deeks漏斗图评估发表偏倚,P<0.05为差异有统计学意义[9]。
2. 结果
2.1 文献检索与纳入
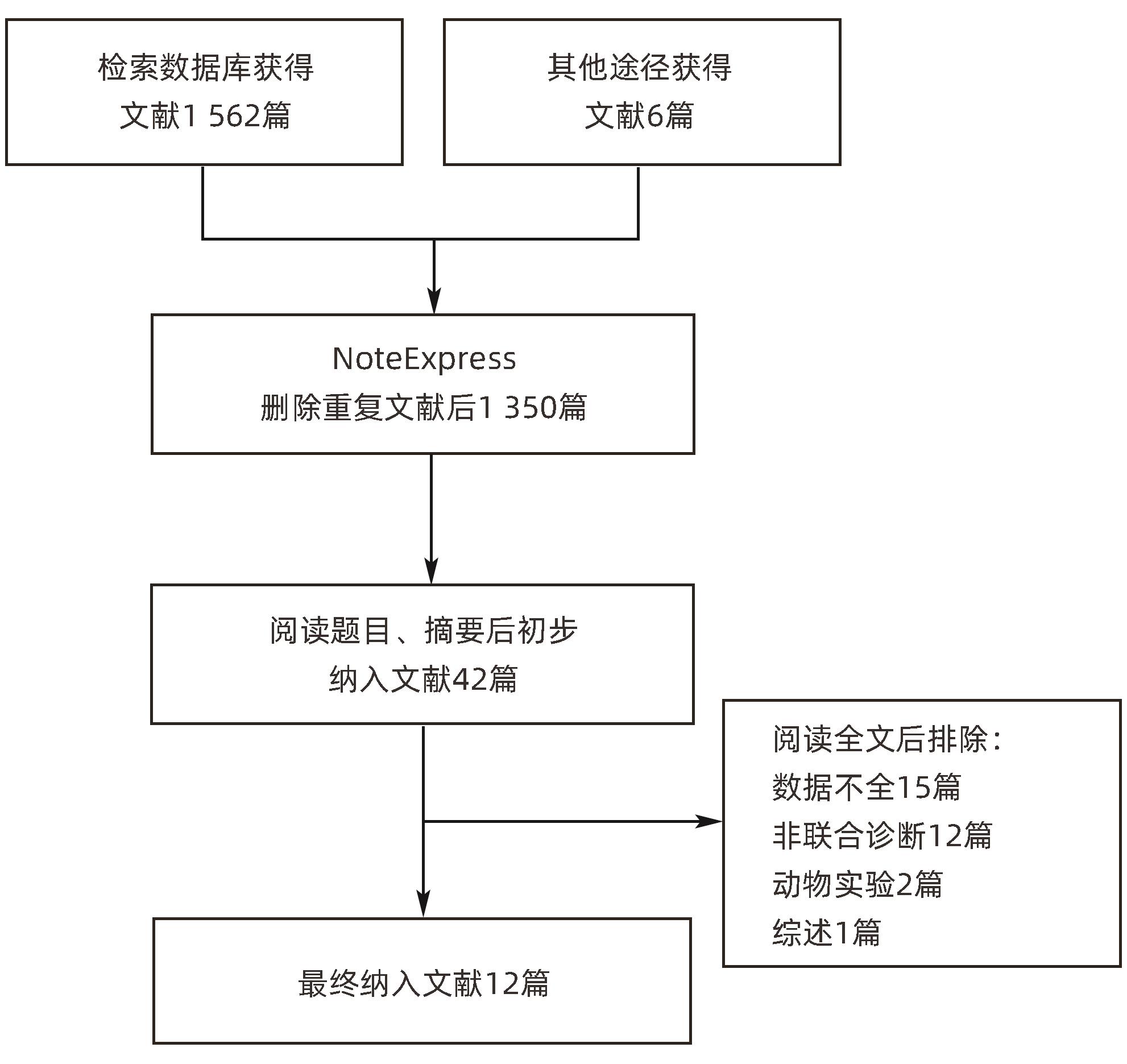
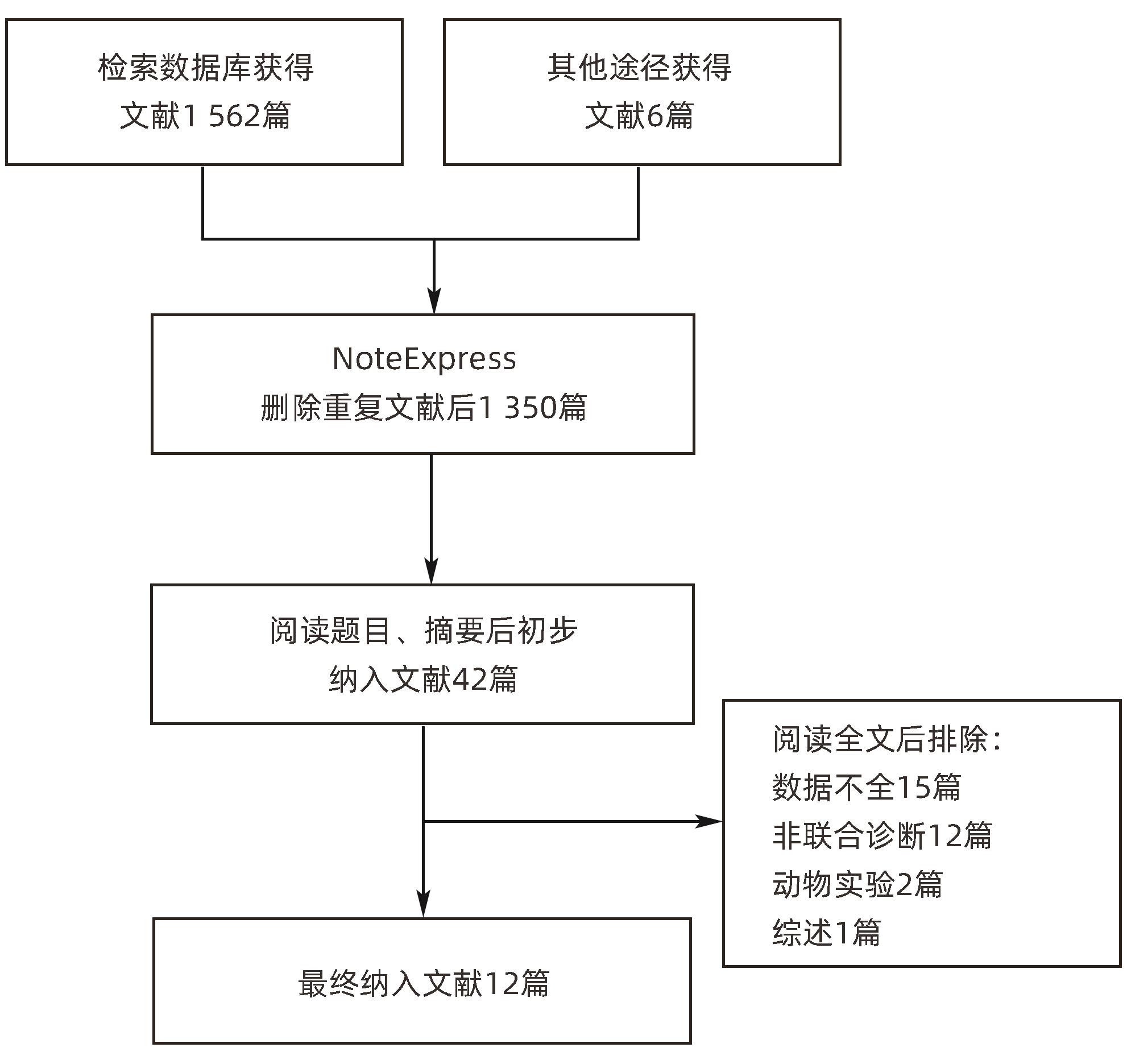
共检索到文献1 562篇,使用NoteExpress软件删除重复文献后,阅读题目、摘要初步纳入42篇文献,排除数据不全及其他不符合纳入标准的30篇文献后,最终纳入12篇文献[10-21],包括8篇中文文献和4篇英文文献,具体筛选流程见图1。
2.2 文献的资料提取与质量评估
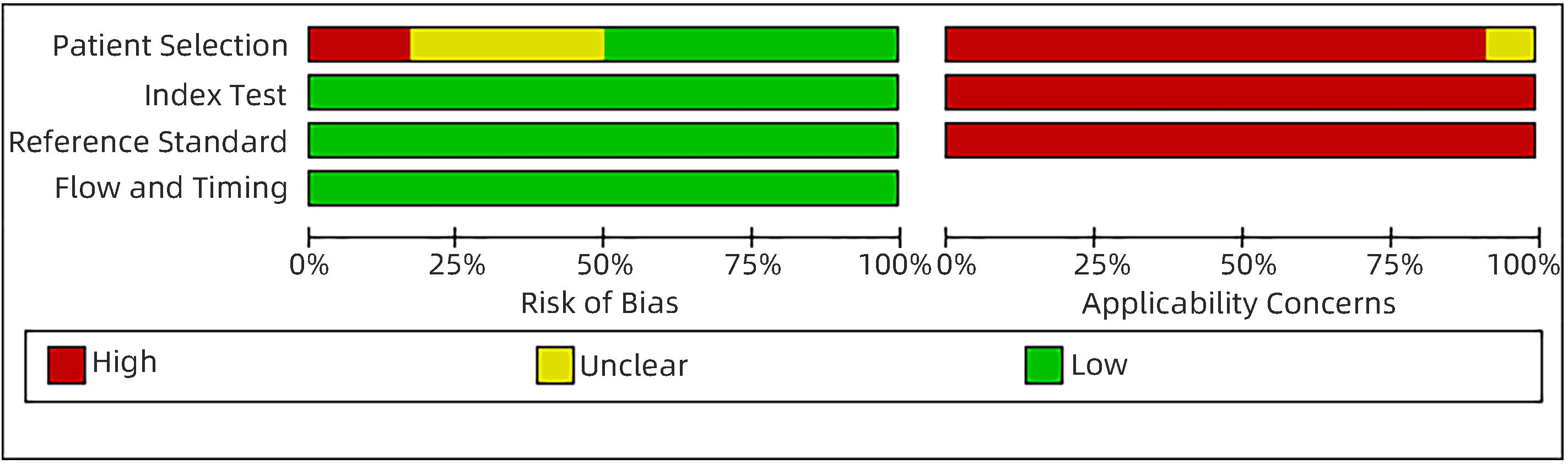
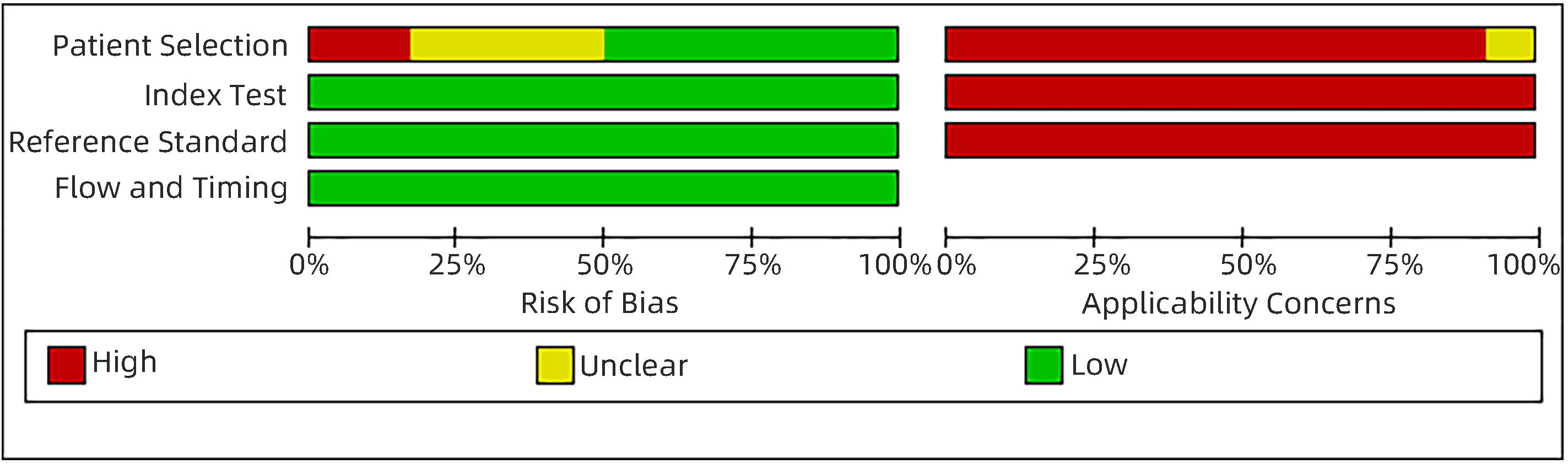
纳入的12篇文献共包括3项回顾性研究和9项前瞻性研究,共1 328例患者,包含1 457个病灶,其中恶性764个,良性693个,阳性率为52.44%,阴性率为47.56%,纳入文献的基本信息见表1。QUADAS-2结果显示,各项研究总体偏倚风险较低,质量评价结果见图2、图3。
表 1 纳入研究的基本信息Table 1. Characteristics of included studies第一作者 发表年份 国家 研究
类型
患者例数(男/女) 病灶个数 病灶个数(恶性/良性) 灵敏度
(%)
特异度
(%)
金标准 TP FP FN TN 宋毅[10] 2015 中国 前瞻性 122(70/52) 52 4 5 61 122(57/65) 91.2 93.8 病理 高莉[11] 2018 中国 前瞻性 80(52/28) 49 3 2 34 88(51/37) 96.1 91.9 病理 王璐[12] 2021 中国 前瞻性 75(43/32) 75 1 3 50 129(78/51) 96.2 98 病理或随访 张家玲[13] 2021 中国 前瞻性 135(83/52) 87 4 4 61 156(91/65) 95.6 93.8 病理或随访 Ruan[14] 2023 中国 回顾性 165(111/54) 114 10 7 40 171(124/47) 94.2 80 病理 潘茜[15] 2022 中国 回顾性 92(47/45) 48 4 4 36 92(52/40) 92.3 90 病理 陈君耀[16] 2022 中国 前瞻性 200(115/85) 33 6 3 158 200(36/164) 91.7 96.3 病理 吴秀琴[17] 2022 中国 回顾性 132(83/49) 47 19 3 63 132(50/82) 94 76.8 病理 Urhuț[18] 2023 罗马尼亚 前瞻性 66(44/22) 45 1 16 10 72(61/11) 73.8 90.9 病理 Hu[19] 2020 中国 前瞻性 136(75/61) 91 3 2 62 158(94/64) 97.8 95.4 病理或影像学 曲美景[20] 2022 中国 前瞻性 79(比例未知) 42 1 1 38 82(43/39) 97.7 97.4 病理或影像学 Wu[21] 2016 中国 前瞻性 46(25/21) 26 5 1 23 55(27/28) 96.3 82.1 病理或影像学 注:TP,真阳性;FP,假阳性;FN,假阴性;TN,真阴性。
2.3 异质性检验
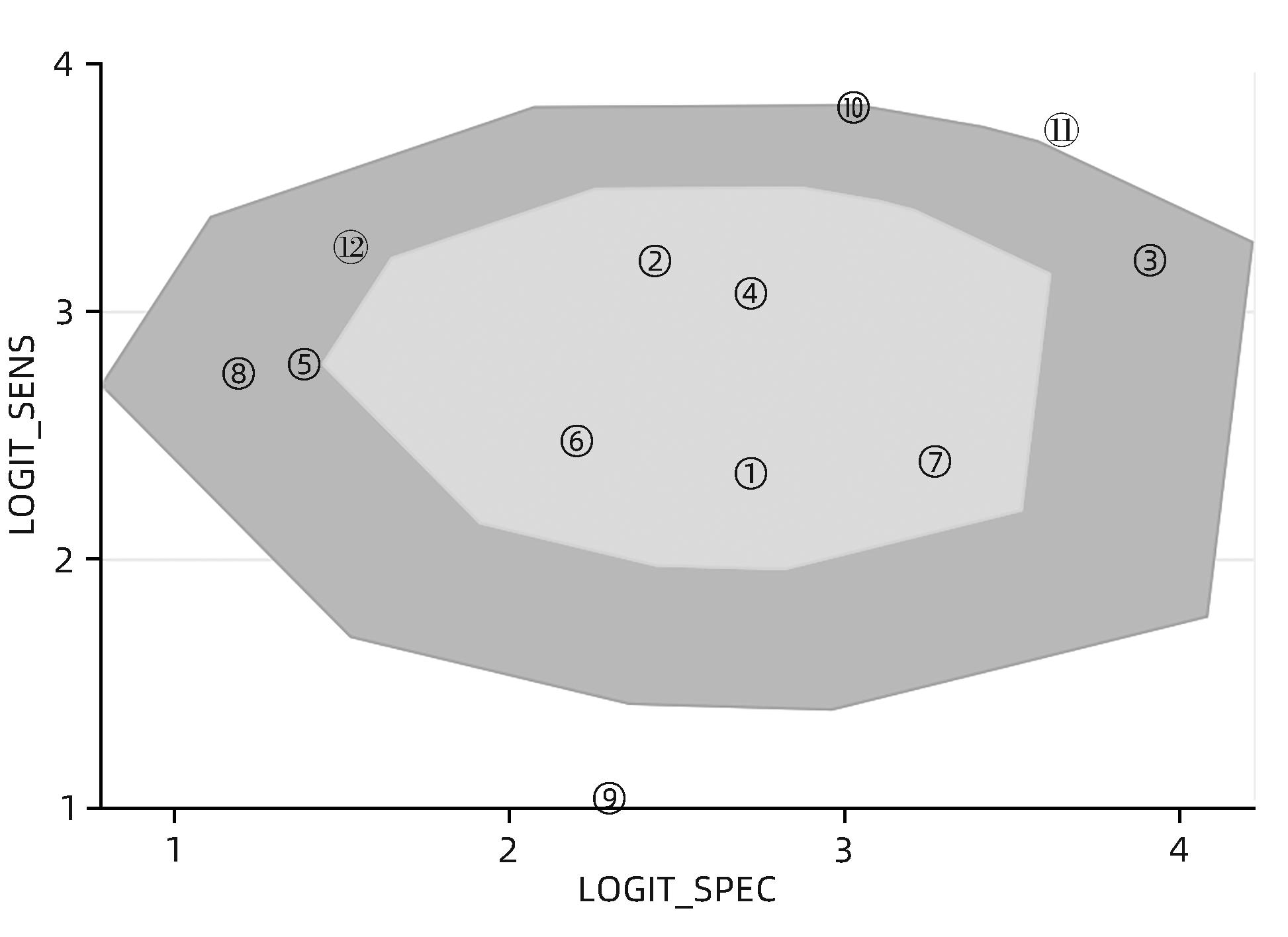
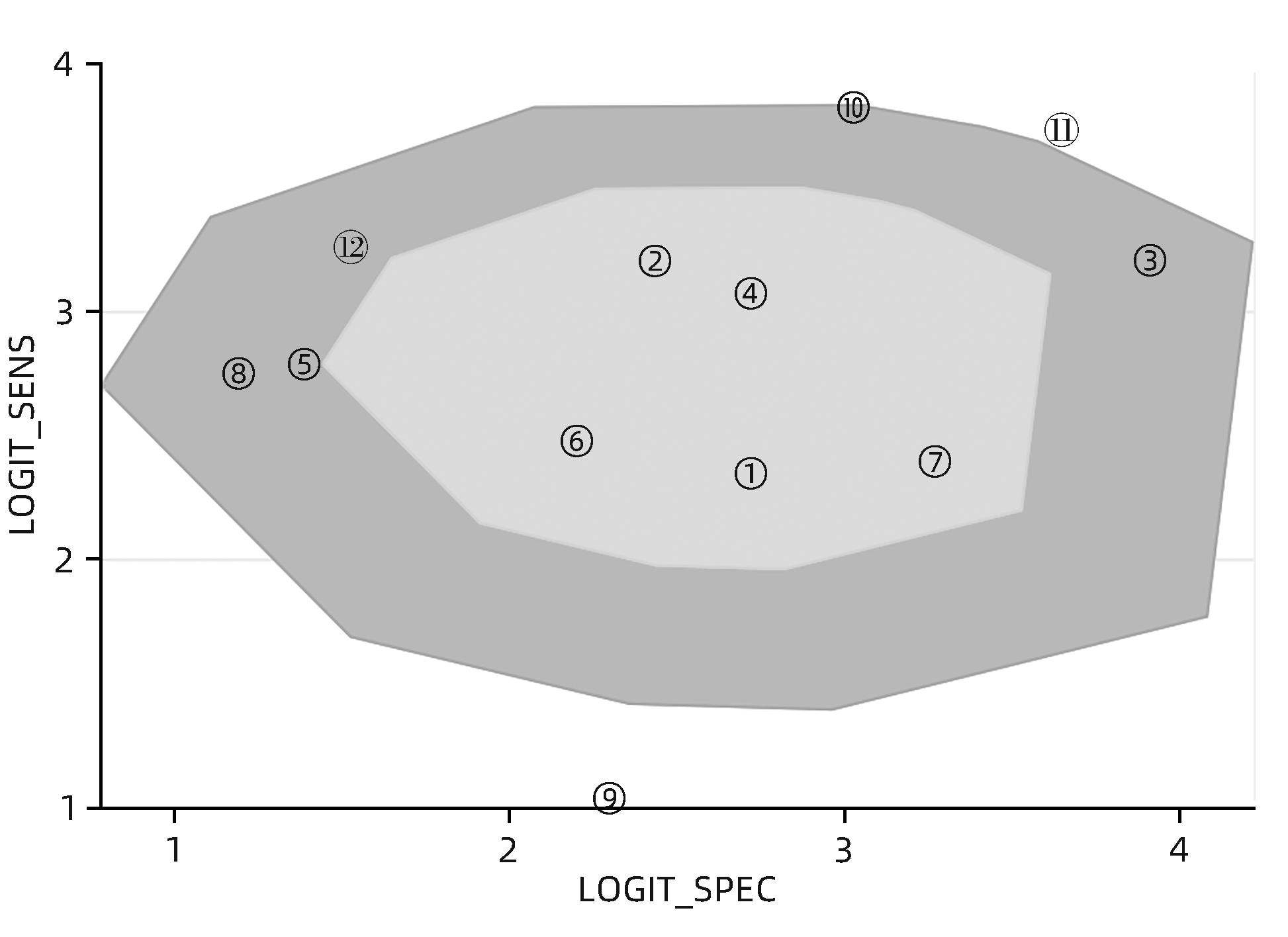
异质性检验结果为Q=54.78,df=11.00,P<0.001,I2=79.92%,95%CI:69.18%~90.66%,提示存在明显异质性;双变量箱式图结果见图4,2篇文献位于中心区域外,10篇文献位于中心区域内,提示各个研究间存在异质性。
2.4 合并效应量结果
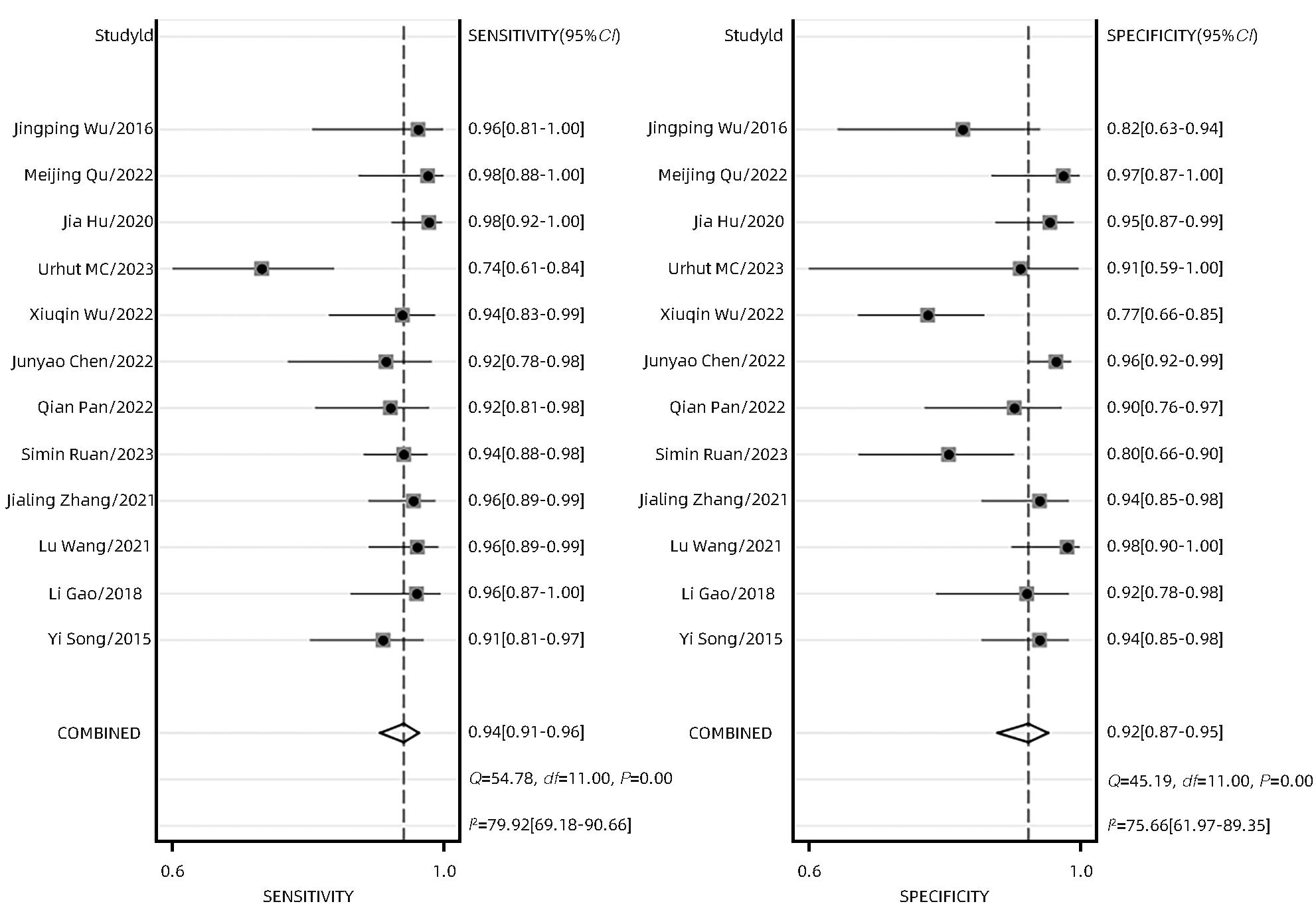
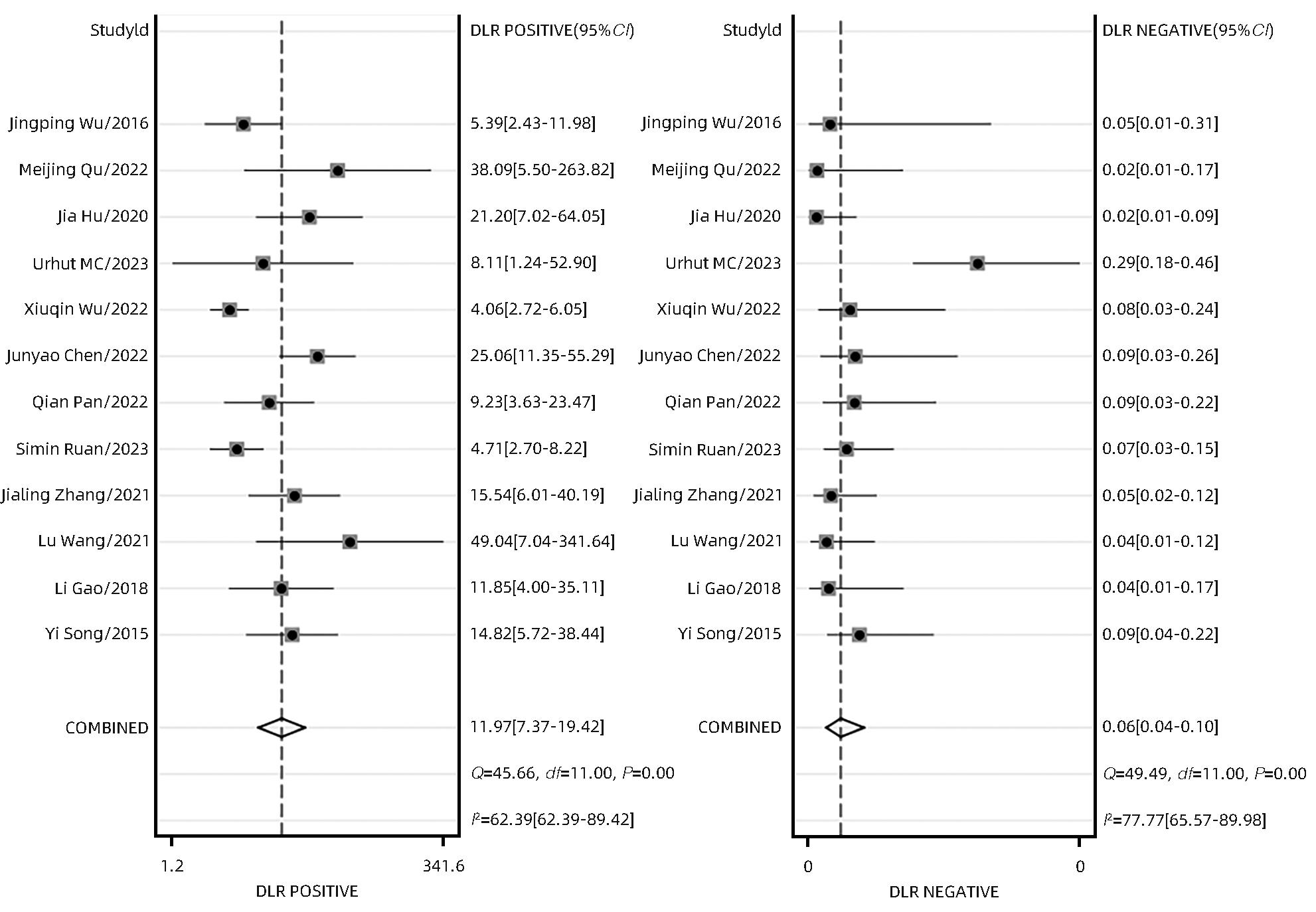
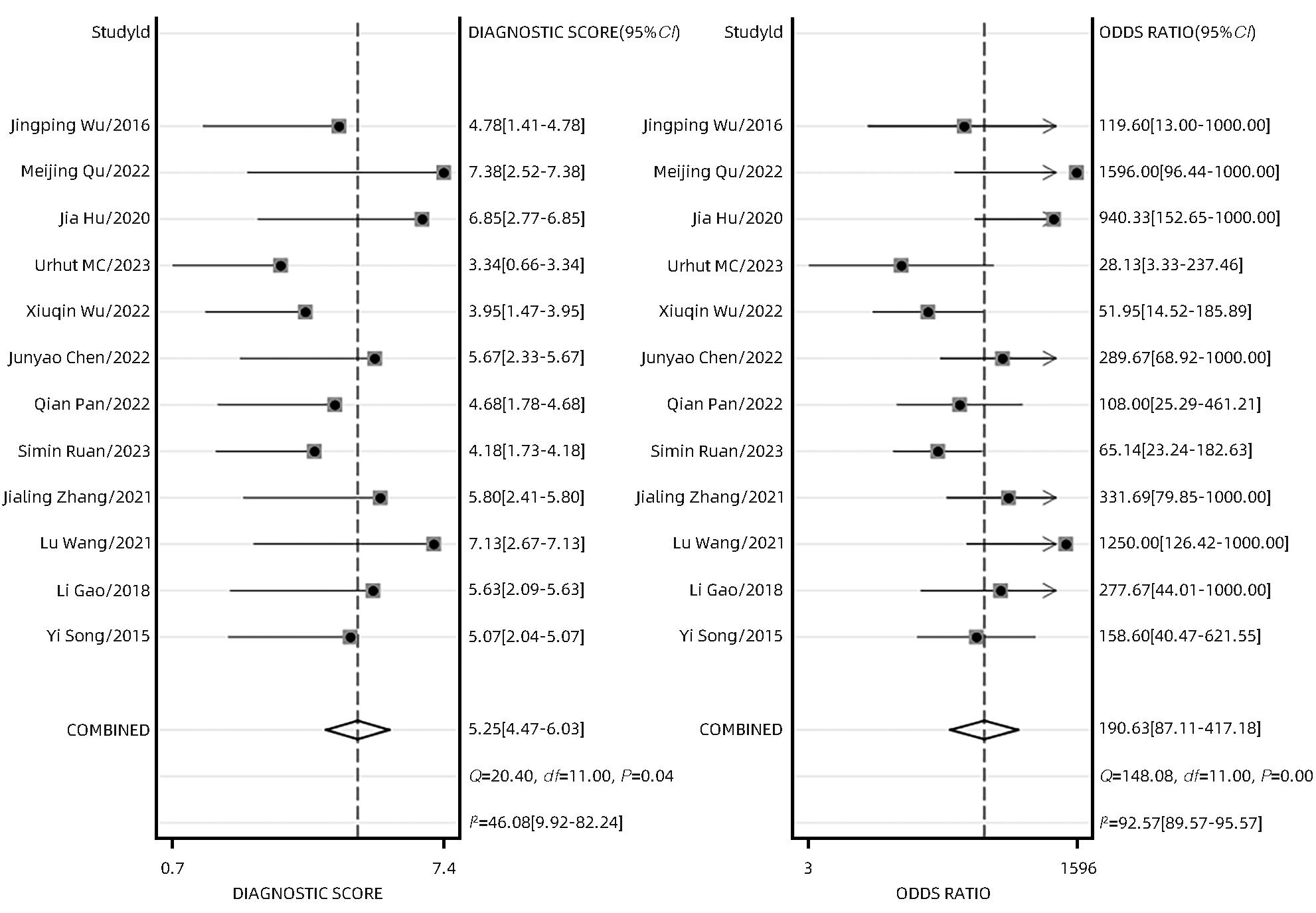
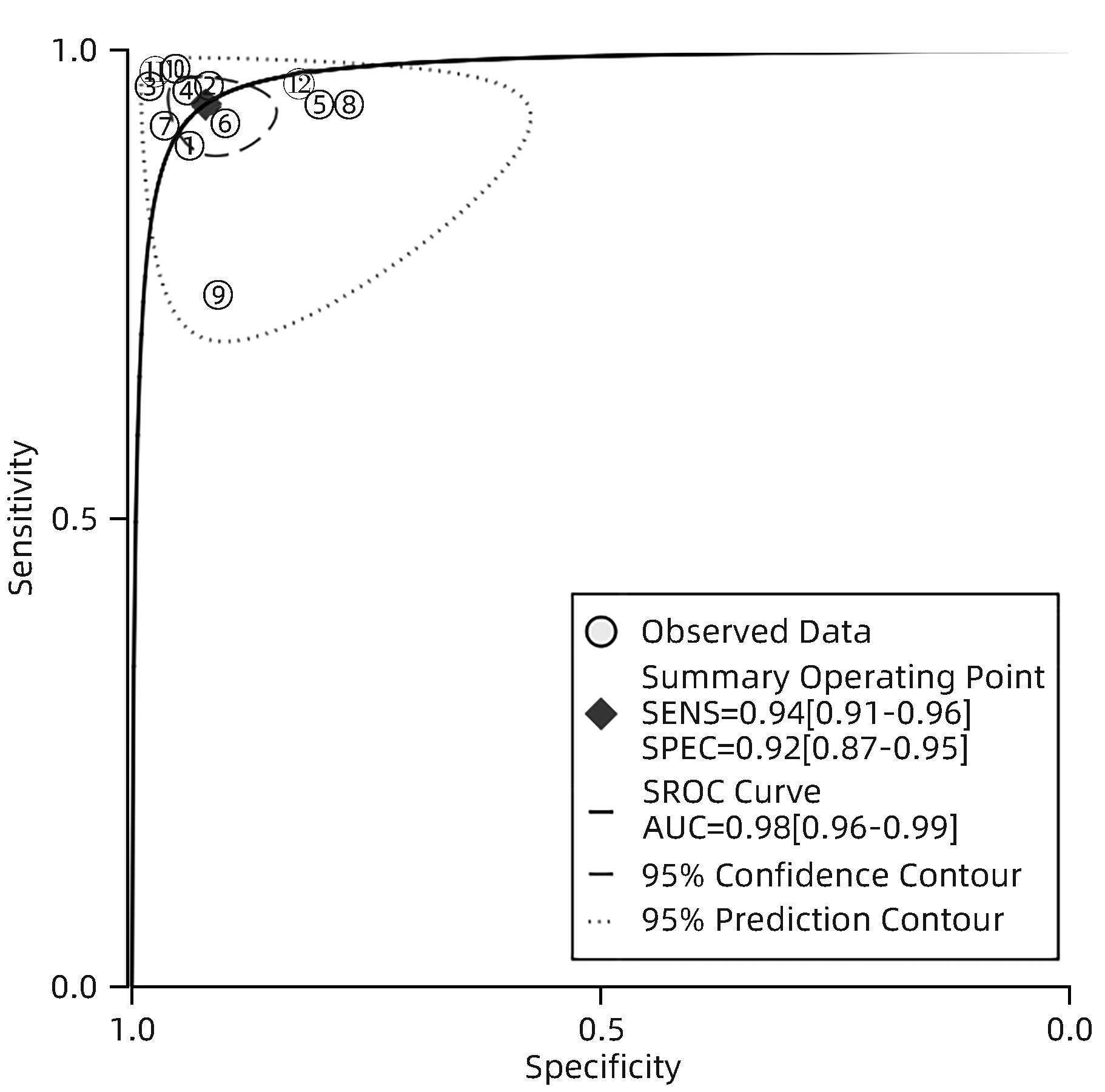
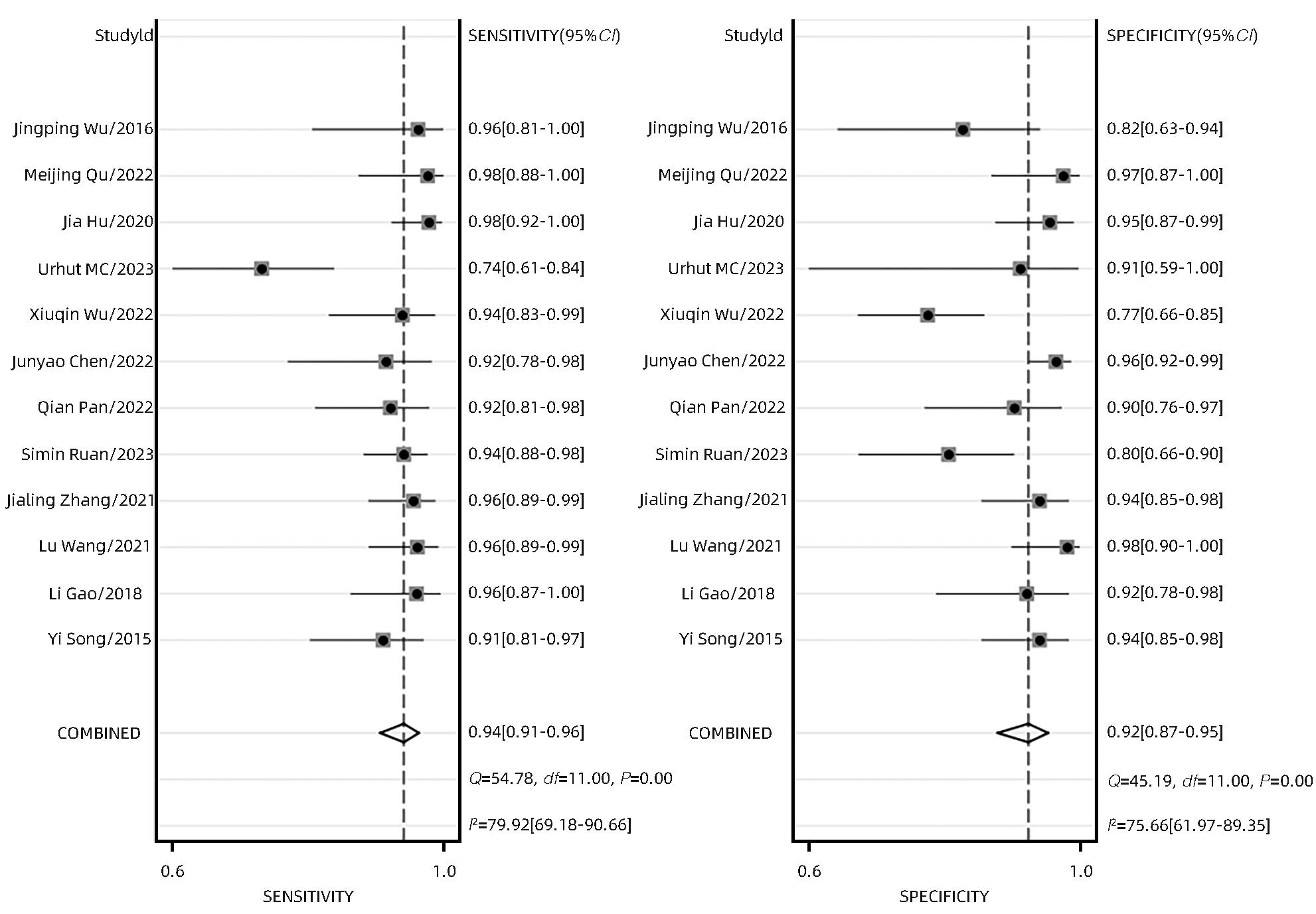
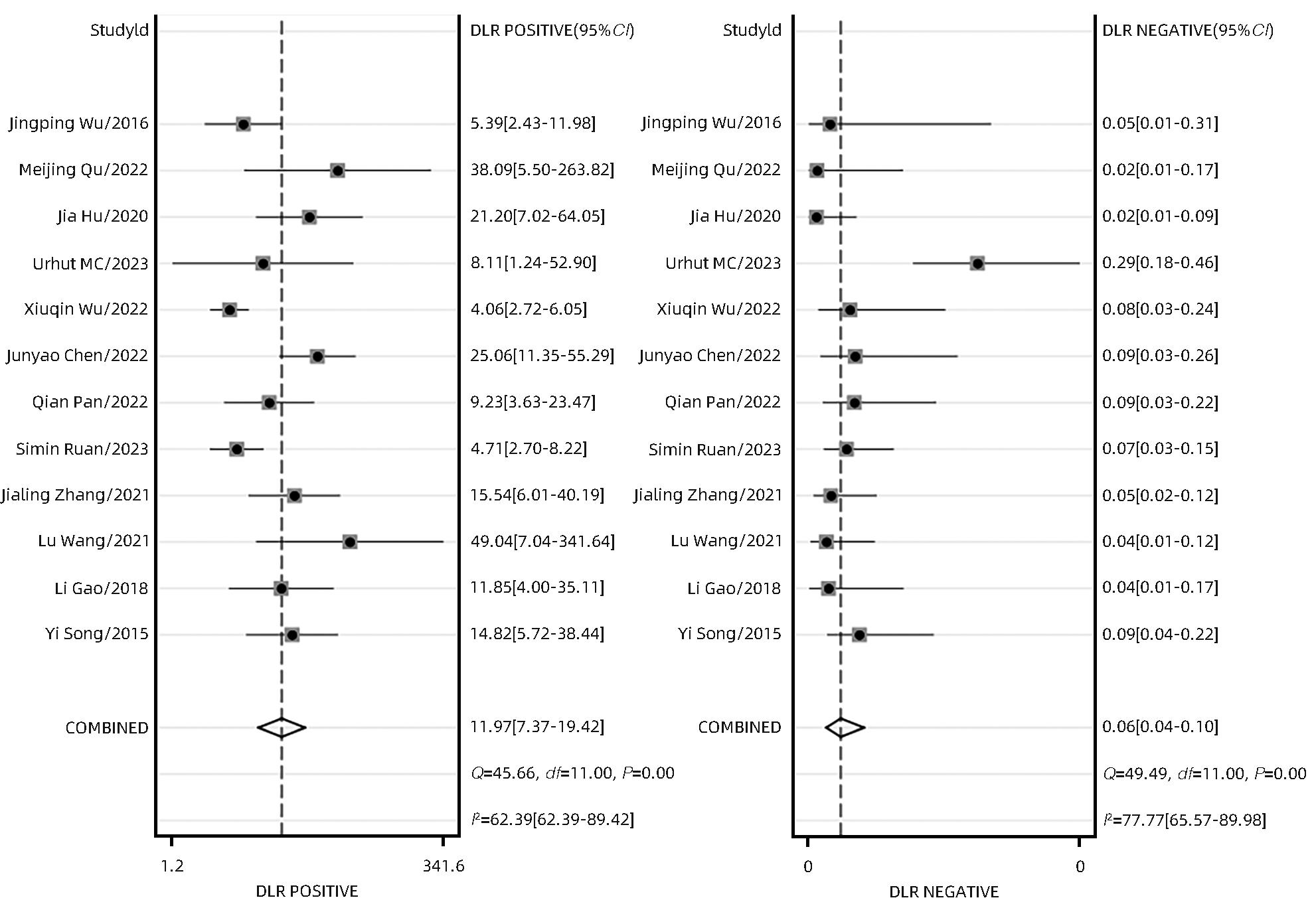
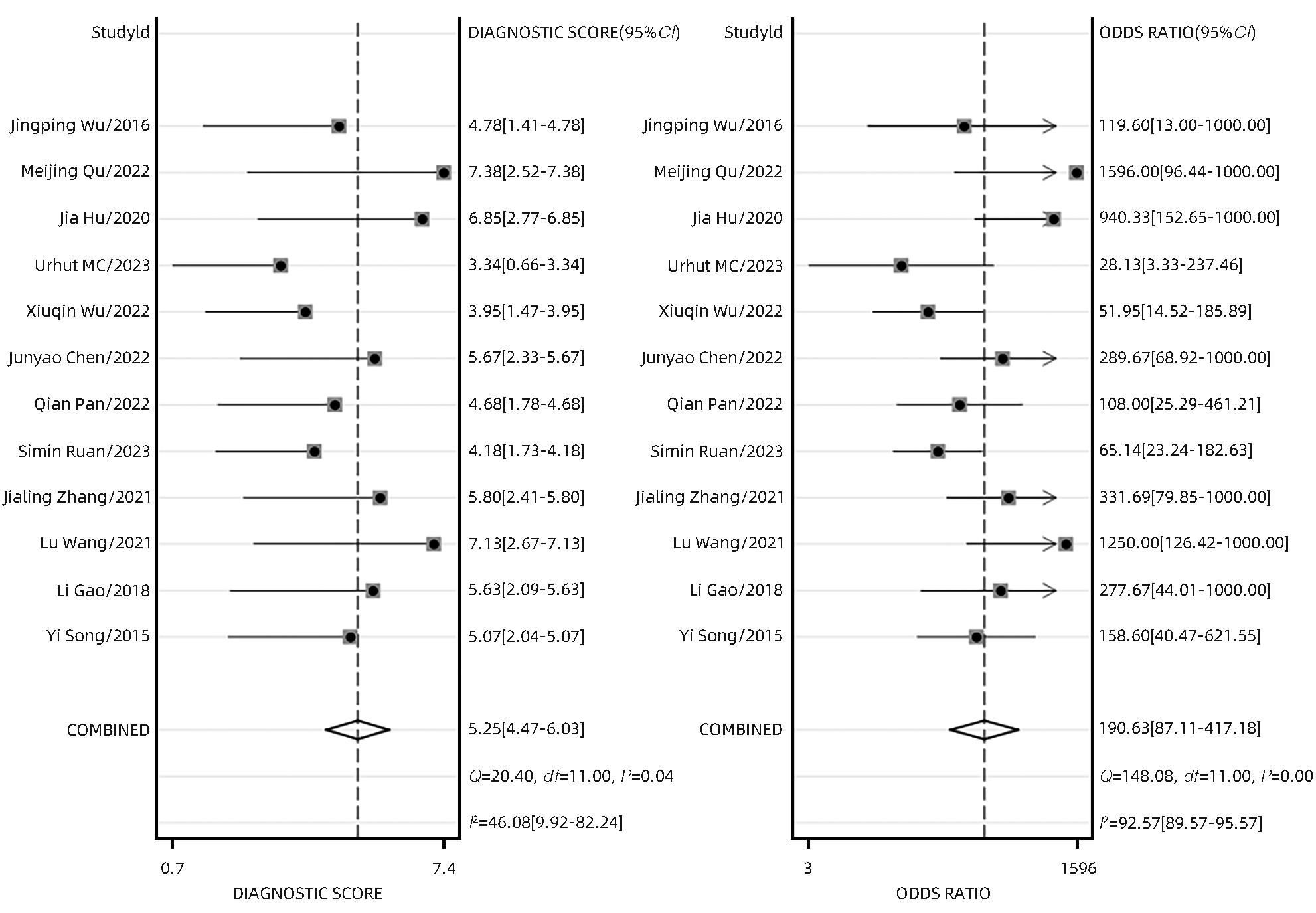
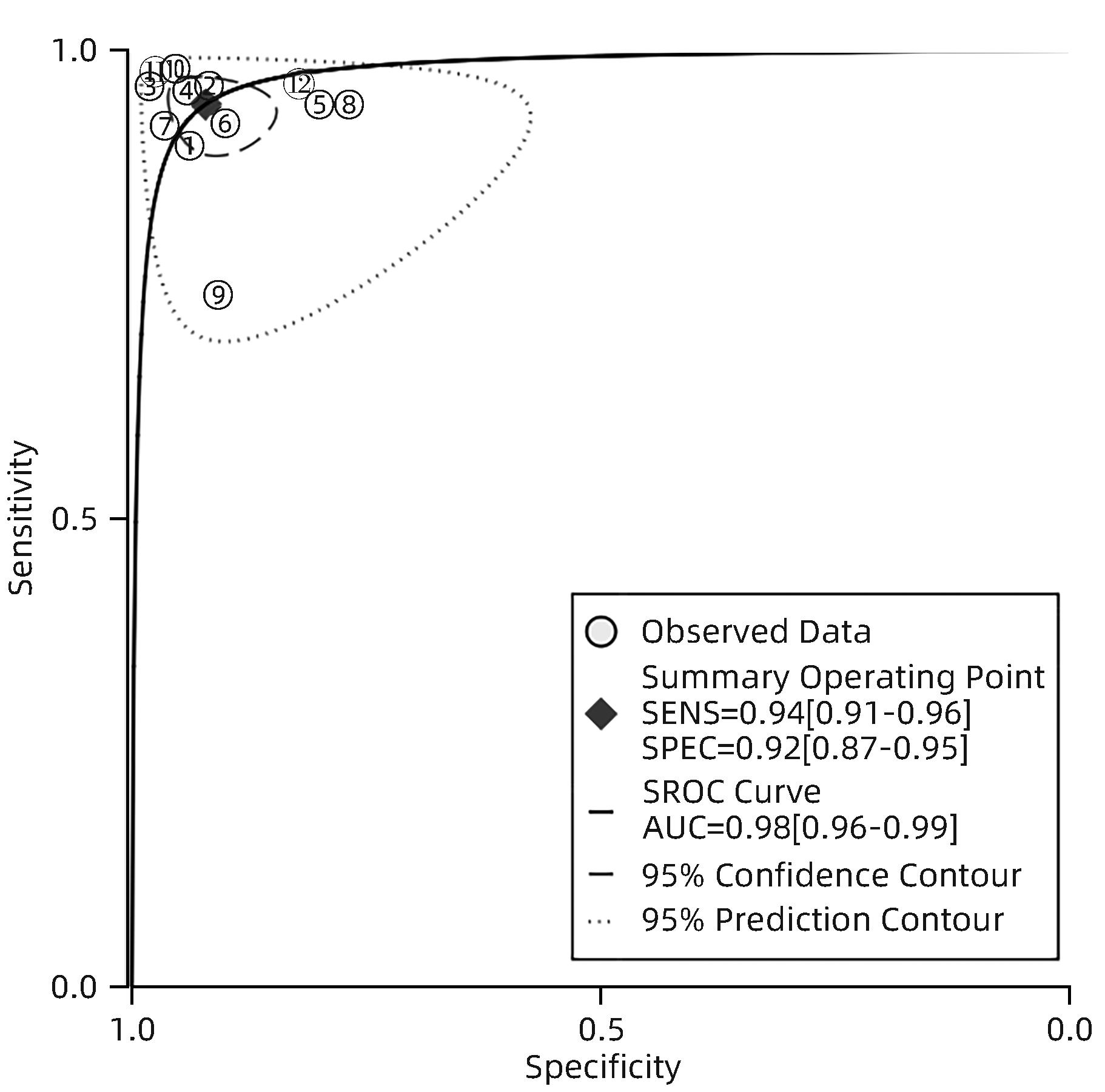
根据异质性评价结果,选用双变量随机效应模型,得到合并灵敏度、特异度、阴性似然比、阳性似然比和诊断比值比分别为0.94(95%CI:0.91~0.96)、0.92(95%CI:0.87~0.95)、12.00(95%CI:7.40~19.40)、0.06(95%CI:0.04~0.10)、191(95%CI:87~417)。SROC曲线以真阳性率为纵轴,假阳性率为横轴,本研究AUC为0.98,结果接近1,说明结果准确度较高(图5~8)。
2.5 发表偏倚的检测
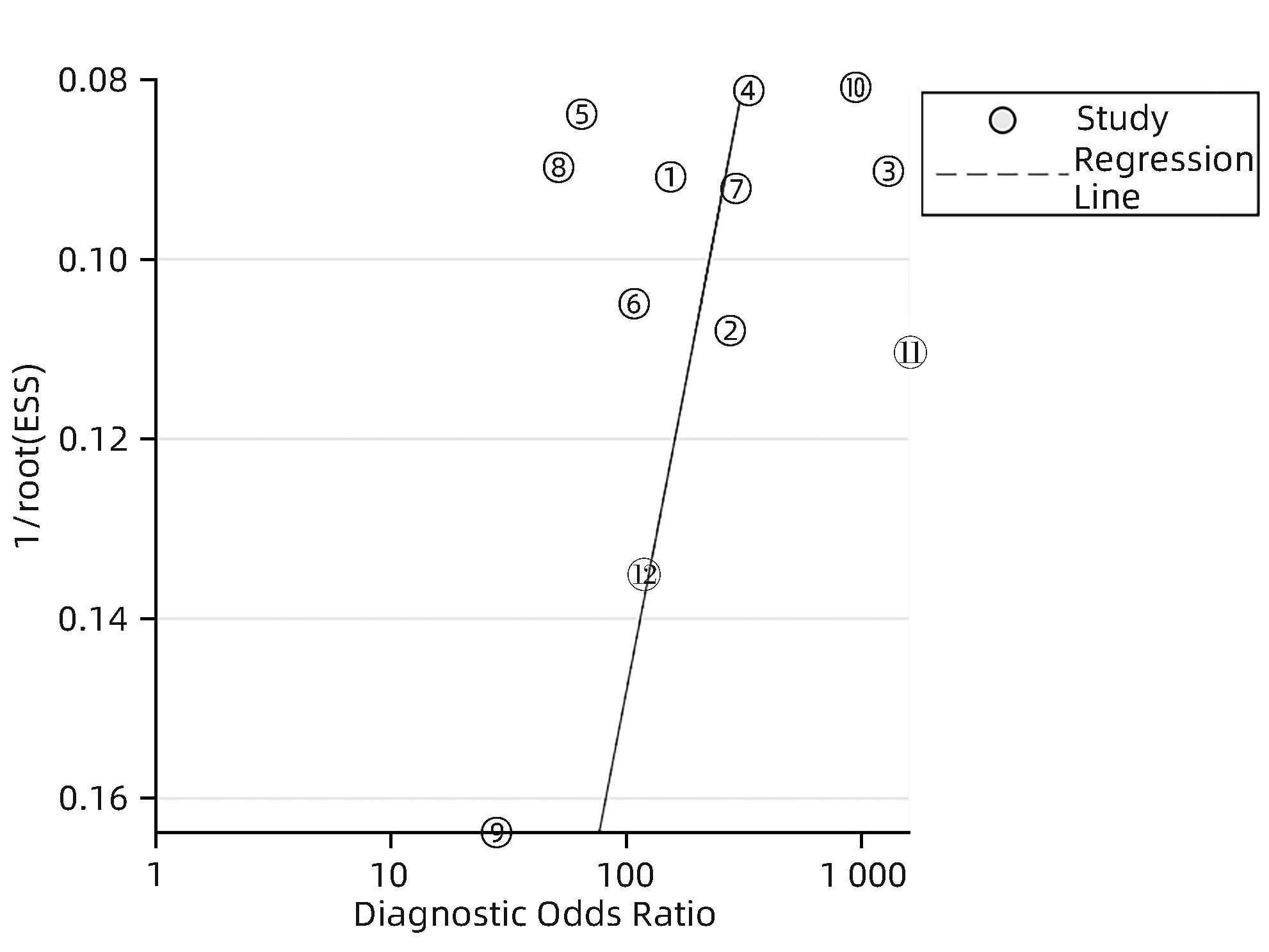
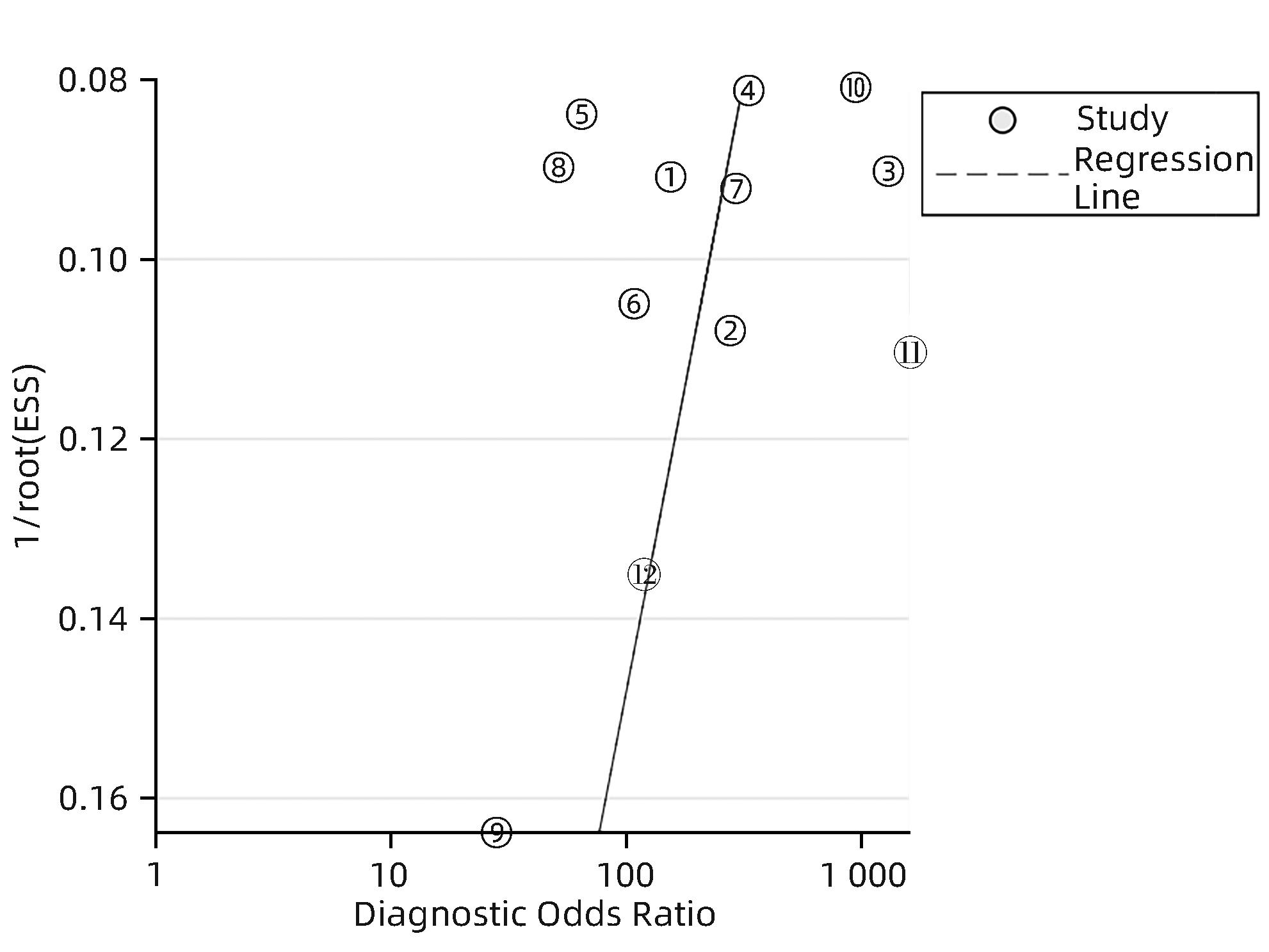
漏斗图可见图形大致对称,定性表明大致无发表偏倚,定量检测结果表明无明显发表偏倚(P=0.425)(图9)。
2.6 敏感性分析
依次删除单篇文献,结果表明,删除Urhuț等[18]的文章后,I2值变为0%,而删除其他文献I2值无明显变化(表2)。
2.7 临床应用价值
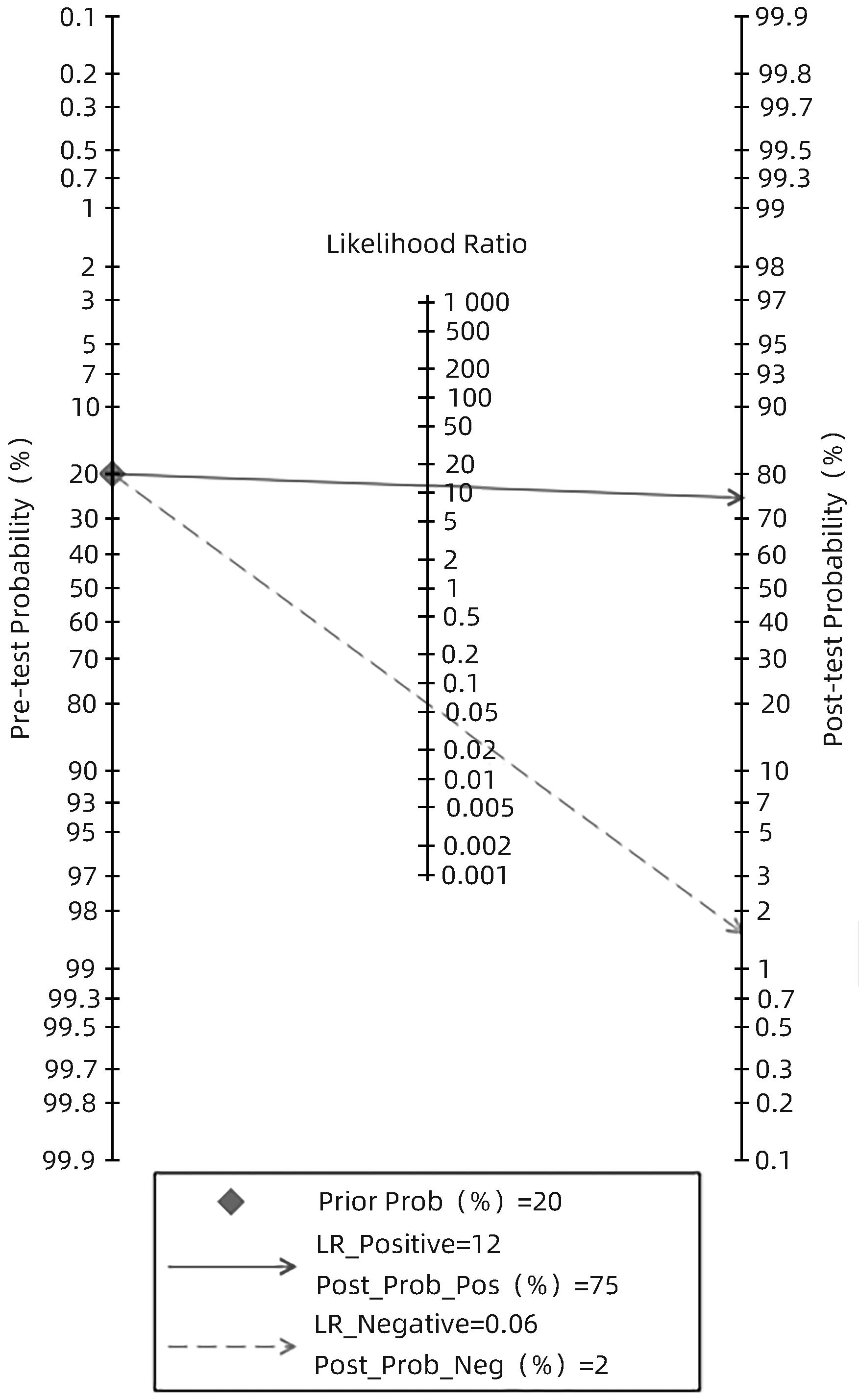
通过Fagan图评价CEUS联合SWE诊断肝脏良恶性肿瘤的临床应用价值(图10),结果显示,验前概率为20%,通过两者联合的诊断方法,其验后概率上升至75%,说明其在临床应用上具有较高的诊断价值。
3. 讨论
肝癌是全球癌症相关死亡的第四大常见原因[22]。随着我国影像技术的高速发展,CEUS和超声弹性成像技术得到了越来越广泛的应用[23]。肝脏恶性病变超声造影动脉期、静脉期、延迟期表现为快进快退,而良性病变表现为快进慢退,从而区分肝脏良恶性肿瘤,但造影结果的判读受医生主观经验的影响[24]。超声弹性成像包括瞬态弹性成像、SWE、应变弹性成像及声辐射力脉冲成像[25-26],其中SWE技术通过测量剪切波速度,得出杨氏模量,反映病灶硬度,对病灶的良恶性判断较为准确[13,27]。然而良性病变与恶性病变的硬度可能存在重叠,从而造成诊断错误。故而将两种超声成像技术联合用以诊断肝脏良恶性肿瘤,可以相互补充,显著提高肝脏良恶性肿瘤的诊断准确度[21]。
本研究的异质性检验结果为I2=79.92%,异质性较为明显,在双变量箱式图中,2篇文章落在中心区域之外,提示各研究间存在异质性,敏感性分析结果显示Urhuț等[18]的研究是异质性的主要来源,可能由于在该研究中,CEUS联合SWE诊断肝肿物的灵敏度较低(73.8%),而其他研究中灵敏度均大于90%。鉴于发现了异质性来源,本研究没有进行亚组分析或者Meta回归分析。异质性除了来源于Urhuț等的研究外,还可能来源于超声仪器不同、操作观察的医生不同,以及造影剂用量不同等。本次Meta分析结果定量显示,将两种影像技术联合起来诊断肝脏良恶性肿瘤的能力较强。本文采用QUADAS-2工具对纳入的文献进行质量评价,质量评价从病例选择、待评价试验、金标准和病例的流程与进展情况四个部分进行,总体而言,本研究纳入的文献质量均较高。本次Meta分析严格按照PRISMA指南进行,合并分析结果必然较单次实验研究结果更为可靠。但本Meta分析可能存在以下局限性:(1)仅检索中英文数据库,且纳入文献大部分为中文文献,可能存在语种偏倚;(2)只纳入12篇文献,样本量偏少可能导致偏倚;(3)在本研究纳入的文献中,金标准除了病理及影像学外,有两项研究[12-13]还包括了临床随访作为金标准,金标准的不统一可能无法避免地引起多重参照偏倚,影响文献质量。
综上所述,CEUS联合超声弹性成像诊断肝脏良恶性肿瘤的能力较强,对于诊断难度较大且不便进行病理检查的肿瘤,两者联合应用可使诊断准确度显著提高,值得临床广泛推广使用。
-
表 1 纳入研究的基本信息
Table 1. Characteristics of included studies
第一作者 发表年份 国家 研究
类型
患者例数(男/女) 病灶个数 病灶个数(恶性/良性) 灵敏度
(%)
特异度
(%)
金标准 TP FP FN TN 宋毅[10] 2015 中国 前瞻性 122(70/52) 52 4 5 61 122(57/65) 91.2 93.8 病理 高莉[11] 2018 中国 前瞻性 80(52/28) 49 3 2 34 88(51/37) 96.1 91.9 病理 王璐[12] 2021 中国 前瞻性 75(43/32) 75 1 3 50 129(78/51) 96.2 98 病理或随访 张家玲[13] 2021 中国 前瞻性 135(83/52) 87 4 4 61 156(91/65) 95.6 93.8 病理或随访 Ruan[14] 2023 中国 回顾性 165(111/54) 114 10 7 40 171(124/47) 94.2 80 病理 潘茜[15] 2022 中国 回顾性 92(47/45) 48 4 4 36 92(52/40) 92.3 90 病理 陈君耀[16] 2022 中国 前瞻性 200(115/85) 33 6 3 158 200(36/164) 91.7 96.3 病理 吴秀琴[17] 2022 中国 回顾性 132(83/49) 47 19 3 63 132(50/82) 94 76.8 病理 Urhuț[18] 2023 罗马尼亚 前瞻性 66(44/22) 45 1 16 10 72(61/11) 73.8 90.9 病理 Hu[19] 2020 中国 前瞻性 136(75/61) 91 3 2 62 158(94/64) 97.8 95.4 病理或影像学 曲美景[20] 2022 中国 前瞻性 79(比例未知) 42 1 1 38 82(43/39) 97.7 97.4 病理或影像学 Wu[21] 2016 中国 前瞻性 46(25/21) 26 5 1 23 55(27/28) 96.3 82.1 病理或影像学 注:TP,真阳性;FP,假阳性;FN,假阴性;TN,真阴性。
-
[1] CHEN QS, SHANG WT, ZENG CT, et al. Theranostic imaging of liver cancer using targeted optical/MRI dual-modal probes[J]. Oncotarget, 2017, 8( 20): 32741- 32751. DOI: 10.18632/oncotarget.15642. [2] ALENEZI AO, KRISHNA S, MENDIRATTA-LALA M, et al. Imaging and management of liver cancer[J]. Semin Ultrasound CT MR, 2020, 41( 2): 122- 138. DOI: 10.1053/j.sult.2019.12.002. [3] HUANG ZR, LI L, HUANG H, et al. Value of multimodal data from clinical and sonographic parameters in predicting recurrence of hepatocellular carcinoma after curative treatment[J]. Ultrasound Med Biol, 2023, 49( 8): 1789- 1797. DOI: 10.1016/j.ultrasmedbio.2023.04.001. [4] WILSON SR, GREENBAUM LD, GOLDBERG BB. Contrast-enhanced ultrasound: what is the evidence and what are the obstacles?[J]. Am J Roentgenol, 2009, 193( 1): 55- 60. DOI: 10.2214/AJR.09.2553. [5] ZHANG P, ZHOU P, TIAN SM, et al. Application of acoustic radiation force impulse imaging for the evaluation of focal liver lesion elasticity[J]. Hepatobiliary Pancreat Dis Int, 2013, 12( 2): 165- 170. DOI: 10.1016/s1499-3872(13)60027-2. [6] MOHER D, LIBERATI A, TETZLAFF J, et al. Preferred reporting items for systematic reviews and meta-analyses: The PRISMA statement[J]. PLoS Med, 2009, 6( 7): e1000097. DOI: 10.1371/journal.pmed.1000097. [7] WADE R, CORBETT M, EASTWOOD A. Quality assessment of comparative diagnostic accuracy studies: Our experience using a modified version of the QUADAS-2 tool[J]. Res Synth Methods, 2013, 4( 3): 280- 286. DOI: 10.1002/jrsm.1080. [8] LI WC, GAO G, LUN ZJ, et al. Identification and treatment of heterogeneity in medical meta-analysis[C]// International Symposium on Computer, Communication, Control and Automation(3CA 2018). Colombo, Sri Lanka. 2018. [9] GJERDEVIK M, HEUCH I. Improving the error rates of the Begg and Mazumdar test for publication bias in fixed effects meta-analysis[J]. BMC Med Res Methodol, 2014, 14: 109. DOI: 10.1186/1471-2288-14-109. [10] SONG Y. The clinical research of real-time shear wave elastography and contrast enhancmented ultrasonography in differential diagnosis of focal liver lesions[D]. Zhengzhou: Zhengzhou University, 2015.宋毅. 实时剪切波弹性成像与超声造影在肝脏局灶性病变中的应用价值[D]. 郑州: 郑州大学, 2015. [11] GAO L, SHI HM, BAI CH. Diagnostic value of contrast-enhanced ultrasound and elastography in benign and malignant liver tumors[J]. Chin Remedies Clin, 2018, 18( 7): 1124- 1125. DOI: 10.11655/zgywylc2018.07.020.高莉, 史红梅, 白彩花. 超声造影与弹性成像在肝脏良恶性肿瘤的诊断价值分析[J]. 中国药物与临床, 2018, 18( 7): 1124- 1125. DOI: 10.11655/zgywylc2018.07.020. [12] WANG L, LU M, WU XB, et al. Value of multimodal ultrasonography in differentiating malignant focal liver lesions from benign ones[J]. J Cancer Contr Treat, 2021, 34( 6): 538- 543. DOI: 10.3969/j.issn.1674-0904.2021.06.009.王璐, 卢漫, 吴晓波, 等. 超声多模态成像鉴别肝脏局灶病变良恶性的价值[J]. 肿瘤预防与治疗, 2021, 34( 6): 538- 543. DOI: 10.3969/j.issn.1674-0904.2021.06.009. [13] ZHANG JL. Clinical value of contrast-enhanced ultrasound and shear wave elastography in the diagnosis of liver tumors[D]. Bengbu: Bengbu Medical College, 2021.张家玲. 超声造影与剪切波弹性成像在肝肿瘤诊断中的临床价值[D]. 蚌埠: 蚌埠医学院, 2021. [14] RUAN SM, HUANG H, CHENG MQ, et al. Shear-wave elastography combined with contrast-enhanced ultrasound algorithm for noninvasive characterization of focal liver lesions[J]. Radiol Med, 2023, 128( 1): 6- 15. DOI: 10.1007/s11547-022-01575-5. [15] PAN Q, WANG SD. Value of contrast-enhanced ultrasound combined with shear wave elastography in the differential diagnosis of benign and malignant nodules in liver parenchyma under the background of liver cirrhosis[J]. J Clin Ultrasound Med, 2022, 24( 2): 119- 122. DOI: 10.3969/j.issn.1008-6978.2022.02.010.潘茜, 王斯达. 超声造影联合剪切波弹性成像对肝硬化背景下肝实质内良恶性结节的鉴别诊断价值[J]. 临床超声医学杂志, 2022, 24( 2): 119- 122. DOI: 10.3969/j.issn.1008-6978.2022.02.010. [16] CHEN JY, LI CY, GUAN HY. Application value of multi-modal ultrasound imaging in screening high risk population of liver cancer[J]. Chin Hepatol, 2022, 27( 3): 288- 291. DOI: 10.14000/j.cnki.issn.1008-1704.2022.03.027.陈君耀, 黎才洋, 官宏勇. 多模态超声成像技术在肝癌高危人群筛查中综合运用策略研究[J]. 肝脏, 2022, 27( 3): 288- 291. DOI: 10.14000/j.cnki.issn.1008-1704.2022.03.027. [17] WU XQ, LING JR, LING J, et al. Application of multimodal ultrasound imaging technology in early screening of liver cancer in middle-aged and elderly people[J]. China Med Equip, 2022, 19( 10): 83- 87. DOI: 10.3969/J.ISSN.1672-8270.2022.10.019.吴秀琴, 凌建容, 凌婧, 等. 多模态超声成像技术在中老年人群早期肝癌筛查中的应用[J]. 中国医学装备, 2022, 19( 10): 83- 87. DOI: 10.3969/J.ISSN.1672-8270.2022.10.019. [18] URHUȚ MC, SĂNDULESCU LD, CIOCÂLTEU A, et al. The clinical value of multimodal ultrasound for the differential diagnosis of hepatocellular carcinoma from other liver tumors in relation to histopathology[J]. Diagnostics, 2023, 13( 20): 3288. DOI: 10.3390/diagnostics13203288. [19] HU J, ZHOU ZY, RAN HL, et al. Diagnosis of liver tumors by multimodal ultrasound imaging[J]. Medicine(Baltimore), 2020, 99( 32): e21652. DOI: 10.1097/MD.0000000000021652. [20] QU MJ. Value of 4-D contrast-enhanced ultrasound combined with shear-wave elastography in the diagnosis of benign and malignant focal liver lesions[D]. Dalian: Dalian Medical University, 2022.曲美景. 四维超声造影联合剪切波弹性成像对肝脏局灶性病变良恶性的诊断价值[D]. 大连: 大连医科大学, 2022. [21] WU JP, SHU R, ZHAO YZ, et al. Comparison of contrast-enhanced ultrasonography with virtual touch tissue quantification in the evaluation of focal liver lesions[J]. J Clin Ultrasound, 2016, 44( 6): 347- 353. DOI: 10.1002/jcu.22335. [22] YANG JD, HAINAUT P, GORES GJ, et al. A global view of hepatocellular carcinoma: Trends, risk, prevention and management[J]. Nat Rev Gastroenterol Hepatol, 2019, 16( 10): 589- 604. DOI: 10.1038/s41575-019-0186-y. [23] CHEN M, GAO N, REN XY, et al. Study on the diagnostic value of contrast-enhanced ultrasound in focal lesions of transplanted liver[J]. Clin J Med Offic, 2023, 51( 3): 279- 281. DOI: 10.16680/j.1671-3826.2023.03.16.陈梅, 高农, 任秀昀, 等. 超声造影对移植肝局灶性病变诊断价值研究[J]. 临床军医杂志, 2023, 51( 3): 279- 281. DOI: 10.16680/j.1671-3826.2023.03.16. [24] LIU FL. Comparison of contrast-enhanced ultrasonography and color Doppler ultrasonography in the diagnosis of hepatic tumors[J]. Guide China Med, 2020, 18( 18): 82- 83. DOI: 10.15912/j.cnki.gocm.2020.18.037.刘凤兰. 超声造影与彩色多普勒超声在肝肿瘤诊断中的效果对比[J]. 中国医药指南, 2020, 18( 18): 82- 83. DOI: 10.15912/j.cnki.gocm.2020.18.037. [25] JOCIUS D, VAJAUSKAS D, SAMUILIS A, et al. Assessing liver fibrosis using 2D-SWE liver ultrasound elastography and dynamic liver scintigraphy with 99mTc-mebrofenin: A comparative prospective single-center study[J]. Medicina(Kaunas), 2023, 59( 3): 479. DOI: 10.3390/medicina59030479. [26] ZHENG Z. Progress in clinical application of shear wave elastography[J]. J Qiqihar Med Univ, 2023, 44( 12): 1166- 1170. DOI: 10.3969/j.issn.1002-1256.2023.12.014.郑直. 剪切波弹性成像临床应用进展[J]. 齐齐哈尔医学院学报, 2023, 44( 12): 1166- 1170. DOI: 10.3969/j.issn.1002-1256.2023.12.014. [27] LIU BR, DONG X, HUANG LP. Diagnostic efficacy of shear wave elastography in evaluating chronic hepatitis B liver fibrosis and related influencing factors[J]. J Clin Hepatol, 2018, 34( 11): 2329- 2333. DOI: 10.3969/j.issn.1001-5256.2018.11.012.刘博儒, 董雪, 黄丽萍. 剪切波弹性成像评估慢性乙型肝炎肝纤维化的价值及影响因素[J]. 临床肝胆病杂志, 2018, 34( 11): 2329- 2333. DOI: 10.3969/j.issn.1001-5256.2018.11.012. -




 PDF下载 ( 0 KB)
PDF下载 ( 0 KB)


 下载:
下载:









 下载:
下载: