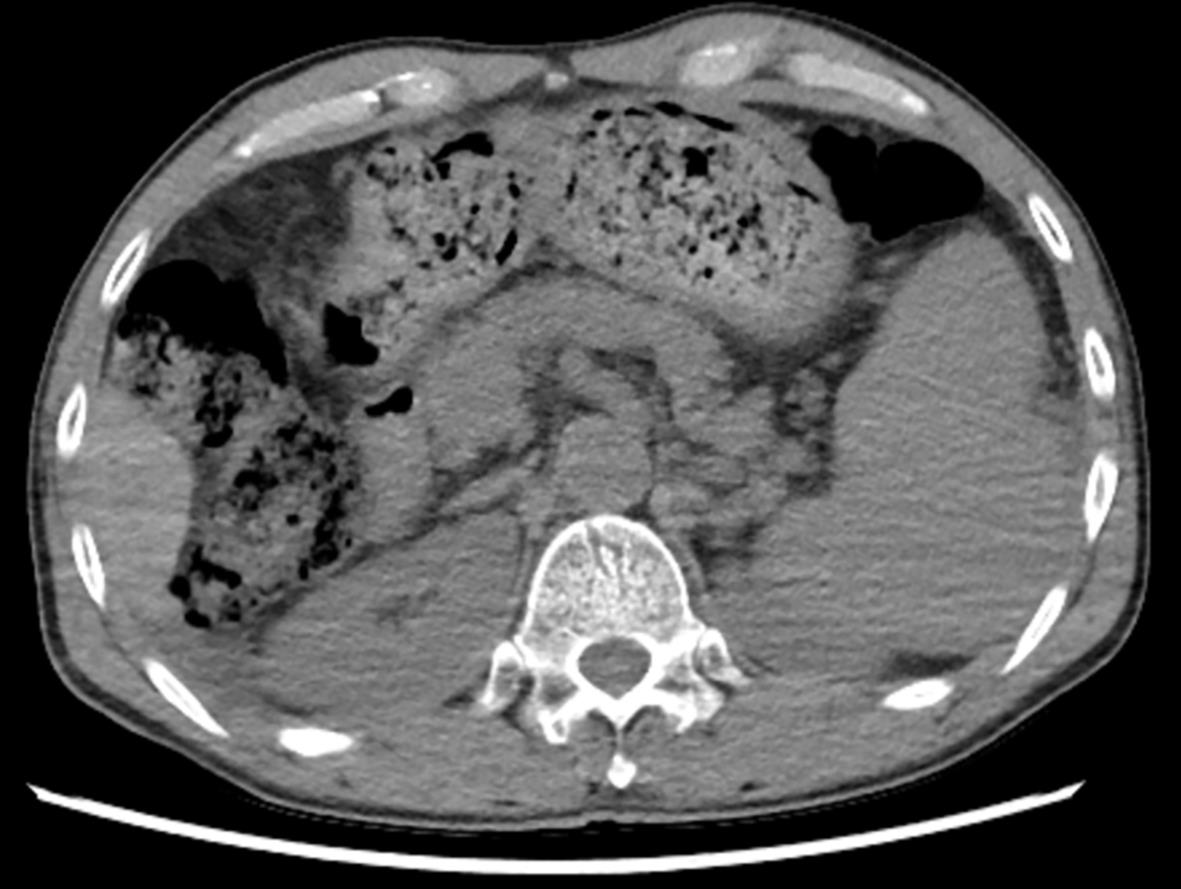
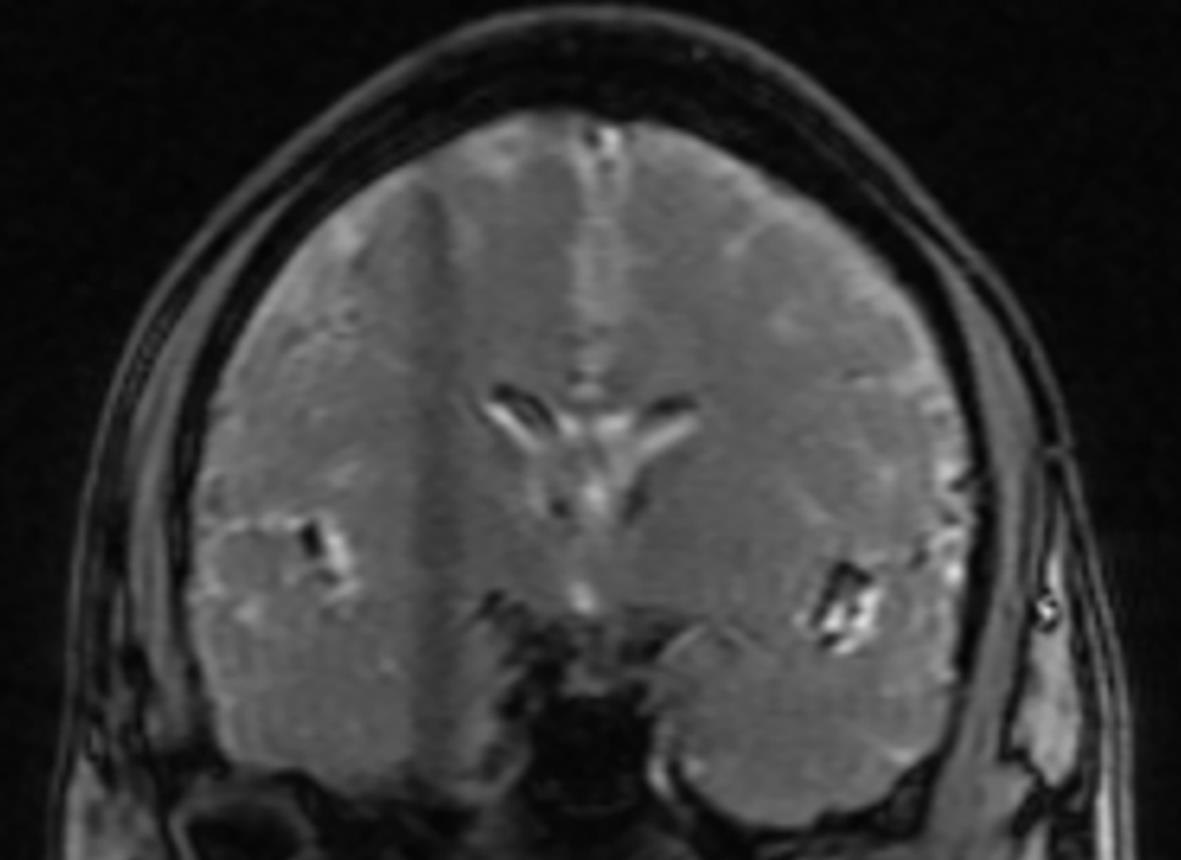
35岁以上肝豆状核变性患者的临床特征分析
DOI: 10.12449/JCH240120
Clinical features of patients with hepatolenticular degeneration aged above 35 years
-
摘要:
目的 总结年龄> 35 岁发病的肝豆状核变性(HLD)患者的临床特征。 方法 回顾性收集2018年4月—2023年4月四川大学华西公共卫生学院诊治的年龄> 35 岁发病的HLD患者的临床资料,根据HLD患者临床症状,分为混合型(n=13)、肝型(n=12)和脑型(n=5)。收集病例的性别、临床表现、确诊年龄、确诊距首发症状时间、家族史等信息;实验室检查,血常规、肝肾功能、血清铜、血清铜蓝蛋白、尿铜、凝血功能等指标以及影像学检查等情况。符合正态分布的计量资料多组间比较采用单因素方差分析;不符合正态分布的计量资料多组间比较采用Kruskal-Wallis H检验。计数资料组间比较采用Fisher确切概率法。 结果 30例HLD患者中,男女比例3∶1,平均年龄(46.13±5.88)岁,角膜K-F环阳性者占43.33%,肝硬化患者高达66.67%。三组间球蛋白、白球比、ALT、凝血酶原时间、国际标准化比率、部分活化凝血活酶时间差异均有统计学意义(F值分别为5.893、4.513、4.424、5.029、5.248、4.942,P值均<0.05)。 结论 35岁以后确诊HLD的患者男性居多,以混合型和肝型为主,肝脏和凝血功能情况较差,对于该年龄段不明原因的肝功能异常及肝硬化,应尽早筛查血清铜蓝蛋白、尿铜等指标,并进行肝肾功能和凝血功能的监测。 Abstract:Objective To investigate the clinical features of patients with hepatolenticular degeneration (HLD) aged above 35 years. Methods A retrospective analysis was performed for the clinical data of the patients with HLD, aged above 35 years, who attended West China School of Public Health, Sichuan University, from April 2018 to April 2023, and according to their clinical symptoms, they were divided into mixed type group with 13 patients, liver type group with 12 patients, and brain type group with 5 patients. Related data were collected, including general information (sex, clinical manifestation, age at confirmed diagnosis, time from initial symptoms to confirmed diagnosis, and family history), laboratory examination (routine blood test, liver and renal function, serum copper, serum ceruloplasmin, urinary copper, and coagulation function), and radiological examination. A one-way analysis of variance was used for comparison of normally distributed continuous data between multiple groups, and the Kruskal-Wallis H test was used for comparison of non-normally distributed continuous data between multiple groups; the Fisher’s exact test was used for comparison of categorical data between groups. Results For the 30 patients with HLD, the male/female ratio was 3∶1, and the mean age was 46.13±5.88 years; the patients with positive Kayser-Fleischer ring of the cornea accounted for 43.33%, and the patients with liver cirrhosis accounted for 66.67%. There were significant differences between the three groups in globulin, albumin/globulin ratio, alanine aminotransferase, prothrombin time, international normalized ratio, and activated partial thromboplastin time (F=5.893, 4.513, 4.424, 5.029, 5.248, and 4.942, all P<0.05). Conclusion Most patients are male among the patients diagnosed with HLD after 35 years of age, with the main clinical types of mixed type and liver type, and such patients tend to have poor liver and coagulation functions. For unexplained liver function abnormalities and liver cirrhosis in this age group, the indicators such as serum ceruloplasmin and urinary copper should be screened as early as possible, and liver and kidney function and coagulation function should be monitored. -
Key words:
- Hepatolenticular Degeneration /
- Diagnosis /
- Adult
-
表 1 不同临床类型HLD患者实验室指标比较
Table 1. Comparison of laboratory parameters among patients with different clinical types of HLD
指标 混合型(n=13) 肝型(n=12) 脑型(n=5) H值 P值 血清铜蓝蛋白(g/L) 0.03(0.02~0.06) 0.06(0.03~0.10) 0.06(0.01~0.15) H=2.761 0.251 尿铜(μg/L) 325.50(175.50~930.50) 352.85(275.25~671.25) 432.50(129.75~958.00) H=0.471 0.790 总蛋白(g/L) 63.49±5.55 68.37±7.80 67.70±3.80 F=2.005 0.154 Alb(g/L) 36.09±5.92 34.62±8.68 42.66±5.06 F=2.337 0.116 球蛋白(g/L) 27.42±4.96 33.75±6.72 25.04±3.91 F=5.893 0.008 白球比 1.39±0.42 1.09±0.42 1.74±0.42 F=4.513 0.020 ALT(U/L) 27.69±16.16 45.17±23.03 20.00±5.83 F=4.424 0.022 AST(U/L) 30.00(22.00~36.00) 50.50(31.75~95.50) 20.00(19.00~28.00) H=9.199 0.010 TBil(μmol/L) 17.00(12.00~28.95) 25.50(16.13~25.50) 14.00(10.40~17.00) H=5.249 0.072 DBil(μmol/L) 7.00(6.00~10.65) 7.05(1.08~25.25) 4.60(4.25~5.00) H=3.491 0.175 IBil(μmol/L) 11.00(6.65~18.30) 15.05(11.28~33.25) 9.00(5.85~12.50) H=5.494 0.064 PT(s) 13.55±1.65 15.63±3.71 11.34±0.89 F=5.029 0.014 INR 1.23±0.15 1.41±0.33 1.01±0.10 F=5.248 0.012 APTT(s) 37.74±5.02 44.48±12.47 29.90±6.28 F=4.942 0.015 注:APTT,活化部分凝血活酶时间。 -
[1] CZŁONKOWSKA A, LITWIN T, DUSEK P, et al. Wilson disease[J]. Nat Rev Dis Primers, 2018, 4: 21. DOI: 10.1038/s41572-018-0018-3. [2] ZHONG HJ, SUN HH, XUE LF, et al. Differential hepatic features presenting in Wilson disease-associated cirrhosis and hepatitis B-associated cirrhosis[J]. World J Gastroenterol, 2019, 25( 3): 378- 387. DOI: 10.3748/wjg.v25.i3.378. [3] KANG CW, WO HY, DONG CC, et al. Analysis of Wilson’s disease presented with osteoarticular symptoms in 14 patients[J]. J Clin Hepatol, 2022, 38( 12): 2814- 2817. DOI: 10.3969/j.issn.1001-5256.2022.12.023.康成为, 沃洪云, 董长超, 等. 14例首发/伴发骨关节症状的肝豆状核变性患者临床特征分析[J]. 临床肝胆病杂志, 2022, 38( 12): 2814- 2817. DOI: 10.3969/j.issn.1001-5256.2022.12.023. [4] LIANG C, BAI L, ZHENG SJ. Research advances in the genotype-phenotype correlation, diagnosis, treatment, and screening of Wilson’s disease[J]. J Clin Hepatol, 2019, 35( 9): 2116- 2119. DOI: 10.3969/j.issn.1001-5256.2019.09.052.梁晨, 白丽, 郑素军. Wilson病基因型-表型关系、诊断、治疗及筛查研究进展[J]. 临床肝胆病杂志, 2019, 35( 9): 2116- 2119. DOI: 10.3969/j.issn.1001-5256.2019.09.052. [5] YU M, REN L, ZHENG M, et al. Delayed diagnosis of wilson’s disease report from 179 newly diagnosed cases in China[J]. Front Neurol, 2022. DOI: 10.3389/fneur.2022.884840. [6] SHI Q, YANG WM. Misdiagnosis analysis of 32 cases of hepatolenticular degeneration[J]. Chin J Integr Med Cardio/cerebrovascular Dis, 2022, 20( 3): 546- 548. DOI: 10.12102/j.issn.1672-1349.2022.03.034.石桥, 杨文明. 32例肝豆状核变性误诊分析[J]. 中西医结合心脑血管病杂志, 2022, 20( 3): 546- 548. DOI: 10.12102/j.issn.1672-1349.2022.03.034. [7] QIU XY, LI H. Clinical misdiagnosis analysis of 14 cases of hepatolenticular degeneration[J]. Clin Misdiagnosis Mistherapy, 2016, 29( 10): 50- 52. DOI: 10.3969/j.issn.1002-3429.2016.10.016.邱星颖, 李华. 肝豆状核变性14例临床误诊分析[J]. 临床误诊误治, 2016, 29( 10): 50- 52. DOI: 10.3969/j.issn.1002-3429.2016.10.016. [8] Inherited Metabolic Liver Disease Collaboration Group, Chinese Society of Hepatology, Chinese Medical Association. Guidelines for the diagnosis and treatment of hepatolenticular degeneration(2022 edition)[J]. Chin J Hepatol, 2022, 30( 1): 9- 20. DOI: 10.3760/cma.j.cn501113-20211217-00603.中华医学会肝病学分会遗传代谢性肝病协作组. 肝豆状核变性诊疗指南(2022年版)[J]. 中华肝脏病杂志, 2022, 30( 1): 9- 20. DOI: 10.3760/cma.j.cn501113-20211217-00603. [9] YANG X. Update on diagnosis and treatment of Wilson disease in China[J]. J Clin Hepatol, 2013, 29( 12): 905- 908. DOI: 10.3969/j.issn.1001-5256.2013.12.008.杨旭. 更新观念, 提高我国肝豆状核变性诊治的临床水平[J]. 临床肝胆病杂志, 2013, 29( 12): 905- 908. DOI: 10.3969/j.issn.1001-5256.2013.12.008. [10] ZHANG W, HUANG J, OU XJ, et al. Key points of AASLD practice guidance for the diagnosis and treatment of Wilson’s disease(2022)[J]. J Clin Hepatol, 2022, 38( 12): 2709- 2711. DOI: 10.3969/j.issn.1001-5256.2022.12.006.张伟, 黄坚, 欧晓娟, 等.《2022年美国肝病学会实践指导: 肝豆状核变性的诊断和治疗》意见要点[J]. 临床肝胆病杂志, 2022, 38( 12): 2709- 2711. DOI: 10.3969/j.issn.1001-5256.2022.12.006. [11] JIANG SS, LUO C, ZHAO R, et al. Case review of Wilson’s disease and correlation analysis of factors except heredity[J]. Chongqing Med, 2016, 45( 8): 1040- 1042. DOI: 10.3969/j.issn.1671-8348.2016.08.011.蒋珊珊, 罗琛, 赵蕊, 等. 肝豆状核变性病例回顾及与遗传以外因素的相关性分析[J]. 重庆医学, 2016, 45( 8): 1040- 1042. DOI: 10.3969/j.issn.1671-8348.2016.08.011. [12] JI L, ZHANG Y, KONG L, et al. Clinical features of Wilson’s disease: An analysis of 83 cases[J]. J Clin Hepatol, 2022, 38( 8): 1843- 1846. DOI: 10.3969/j.issn.1001-5256.2022.08.023.纪雷, 张莹, 孔丽, 等. 83例肝豆状核变性患者的临床特征分析[J]. 临床肝胆病杂志, 2022, 38( 8): 1843- 1846. DOI: 10.3969/j.issn.1001-5256.2022.08.023. [13] COFFEY AJ, DURKIE M, HAGUE S, et al. A genetic study of Wilson’s disease in the United Kingdom[J]. Brain, 2013, 136( Pt 5): 1476- 1487. DOI: 10.1093/brain/awt035. [14] GROMADZKA G, WIERZBICKA D, LITWIN T, et al. Difference in iron metabolism may partly explain sex-related variability in the manifestation of Wilson’s disease[J]. J Trace Elem Med Biol, 2020, 62: 126637. DOI: 10.1016/j.jtemb.2020.126637. [15] TIAN Y, GONG GZ, YANG X, et al. Diagnosis and management of fulminant Wilson’s disease: A single center’s experience[J]. World J Pediatr, 2016, 12( 2): 209- 214. DOI: 10.1007/s12519-015-0026-2. [16] FERNANDO M, van MOURIK I, WASSMER E, et al. Wilson disease in children and adolescents[J]. Arch Dis Child, 2020, 105( 5): 499- 505. DOI: 10.1136/archdischild-2018-315705. [17] MULLIGAN C, BRONSTEIN JM. Wilson disease: An overview and approach to management[J]. Neurol Clin, 2020, 38( 2): 417- 432. DOI: 10.1016/j.ncl.2020.01.005. [18] SCHILSKY ML, ROBERTS EA, BRONSTEIN JM, et al. A multidisciplinary approach to the diagnosis and management of Wilson disease: Executive summary of the 2022 Practice Guidance on Wilson disease from the American Association for the Study of Liver Diseases[J]. Hepatology, 2023, 77( 4): 1428- 1455. DOI: 10.1002/hep.32805. [19] CHANPONG A, DHAWAN A. Wilson disease in children and young adults-State of the art[J]. Saudi J Gastroenterol, 2022, 28( 1): 21- 31. DOI: 10.4103/sjg.sjg_501_21. [20] LITWIN T, DUSEK P, SZAFRAŃSKI T, et al. Psychiatric manifestations in Wilson’s disease: Possibilities and difficulties for treatment[J]. Ther Adv Psychopharmacol, 2018, 8( 7): 199- 211. DOI: 10.1177/2045125318759461. [21] European Association for Study of Liver. EASL clinical practice guidelines: Wilson’s disease[J]. J Hepatol, 2012, 56( 3): 671- 685. DOI: 10.1016/j.jhep.2011.11.007. [22] CZŁONKOWSKA A, TARNACKA B, LITWIN T, et al. Wilson’s disease-cause of mortality in 164 patients during 1992-2003 observation period[J]. J Neurol, 2005, 252( 6): 698- 703. DOI: 10.1007/s00415-005-0720-4. [23] WEISS KH, van de MOORTELE M, GOTTHARDT DN, et al. Bone demineralisation in a large cohort of Wilson disease patients[J]. J Inherit Metab Dis, 2015, 38( 5): 949- 956. DOI: 10.1007/s10545-015-9815-y. [24] KORMAN JD, VOLENBERG I, BALKO J, et al. Screening for Wilson disease in acute liver failure: A comparison of currently available diagnostic tests[J]. Hepatology, 2008, 48( 4): 1167- 1174. DOI: 10.1002/hep.22446. [25] RYAN A, NEVITT SJ, TUOHY O, et al. Biomarkers for diagnosis of Wilson’s disease[J]. Cochrane Database Syst Rev, 2019, 2019( 11): CD012267. DOI: 10.1002/14651858.cd012267. [26] FERENCI P, OTT P. Wilson’s disease: Fatal when overlooked, curable when diagnosed[J]. J Hepatol, 2019, 71( 1): 222- 224. DOI: 10.1016/j.jhep.2019.02.002. [27] SHRIBMAN S, MARJOT T, SHARIF A, et al. Investigation and management of Wilson’s disease: A practical guide from the British Association for the Study of the Liver[J]. Lancet Gastroenterol Hepatol, 2022, 7( 6): 560- 575. DOI: 10.1016/s2468-1253(22)00004-8. -



 PDF下载 ( 819 KB)
PDF下载 ( 819 KB)

 下载:
下载: