维生素D缺乏对非酒精性脂肪性肝炎患者FIB-4指数及病情严重程度的影响
DOI: 10.3969/j.issn.1001-5256.2022.06.015
Influence of vitamin D deficiency on fibrosis-4 index and disease severity in patients with nonalcoholic steatohepatitis
-
摘要:
目的 探讨维生素D缺乏对非酒精性脂肪性肝炎(NASH)的影响。 方法 选取2020年1月—2021年10月冬春季在长沙市第一医院感染科住院治疗的NASH患者,根据血清1, 25(OH)2D3水平分为3组:A组为1, 25(OH)2D3缺乏组(<20 ng/mL),B组为1, 25(OH)2D3不足组(20~30 ng/mL),C组为1, 25(OH)2D3充足组(>30 ng/mL)。比较3组患者血清1, 25(OH)2D3、ALT、AST、TBil、TC、TG、IL-18、IL-37水平和肝脏病理分级的差异,计算FIB-4指数。计量资料多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。计数资料组间比较采用χ2检验。相关性采用Pearson相关分析。 结果 共纳入NASH患者120例,A、B、C 3组各40例。与A组比较,B、C两组患者1, 25(OH)2D3、IL-37水平升高,而FIB-4指数和ALT、AST、TBil、TC、TG、IL-18水平降低,差异均有统计学意义(P值均<0.05)。与B组比较,C组患者1, 25(OH)2D3、IL-37水平升高,FIB-4指数和ALT、AST、TC、TG、IL-18水平降低,差异均有统计学意义(P值均<0.05)。相关性分析结果显示,1, 25(OH)2D3与ALT(r=-0.84,P<0.001)、AST(r=-0.77,P<0.001)、TBil(r=-0.32,P<0.001)、TC(r=-0.45,P<0.001)、TG(r=-0.42,P<0.001)、IL-18(r=-0.40,P<0.001)及FIB-4指数(r=-0.62,P<0.001)均呈负相关,而与IL-37(r=0.59,P<0.001)呈正相关。与A组相比,B、C组中与重度脂肪变(χ2=51.46,P<0.001)、桥接纤维化与早期肝硬化(χ2=36.59,P<0.001)、桥接坏死与大片坏死(χ2=37.28,P<0.001)比例下降。光镜示A组肝细胞广泛气球样变,大量大泡性为主的脂滴,肝板排列紊乱,淋巴细胞浸润,局灶桥接纤维化;B组多数为点灶坏死,门静脉周围纤维化,脂滴大小不等,少量中性粒细胞浸润,部分肝细胞气球样变;C组少量肝细胞气球样变,局灶窦周纤维化,少数点灶坏死,肝细胞胞质可见少量脂滴。 结论 维生素D水平越低,NASH患者肝损伤、肝纤维化程度越明显,检测维生素D有助于评估NASH患者病情进展情况。 Abstract:Objective To investigate the influence of vitamin D deficiency on nonalcoholic steatohepatitis (NASH). Methods The patients with NASH who were hospitalized in Department of Infectious Diseases, The First Hospital of Changsha, from January 2020 to October 2021 were enrolled, and according to the serum level of 1, 25(OH)2D3, they were divided into group A with 1, 25(OH)2D3 deficiency (< 20 ng/mL), group B with 1, 25(OH)2D3 insufficiency (20-30 ng/mL), and group C with sufficient 1, 25(OH)2D3 (> 30 ng/mL). The three groups were compared in terms of the serum levels of 1, 25(OH)2D3, alanine aminotransferase (ALT), aspartate aminotransferase (AST), total bilirubin (TBil), total cholesterol (TC), triglyceride (TG), interleukin-18 (IL-18), and interleukin-37 (IL-37) and liver pathological grade, and fibrosis-4 (FIB-4) index was calculated. A one-way analysis of variance was used for comparison of continuous data between multiple groups, and the least significant difference t-test was used for further comparison between two groups; the chi-square test was used for comparison of categorical data between groups. A Pearson correlation analysis was also performed. Results A total of 120 NASH patients were enrolled, with 40 patients in each group. Compared with group A, groups B and C had significant increases in the levels of 1, 25(OH)2D3 and IL-37 and significant reductions in FIB-4 index and the levels of ALT, AST, TBil, TC, TG, and IL-18 (all P < 0.05). Compared with group B, group C had significant increases in the levels of 1, 25(OH)2D3 and IL-37 and significant reductions in FIB-4 index and the levels of ALT, AST, TC, TG, and IL-18 (all P < 0.05). The correlation analysis showed that 1, 25(OH)2D3 was negatively correlated with ALT (r=-0.84, P < 0.001), AST (r=-0.77, P < 0.001), TBil (r=-0.32, P < 0.001), TC (r=-0.45, P < 0.001), TG (r=-0.42, P < 0.001), IL-18 (r=-0.40, P < 0.001), and FIB-4 index (r=-0.62, P < 0.001), and it was positively correlated with IL-37 (r=0.59, P < 0.001). Compared with group A, groups B and C had significant reductions in the proportion of patients with severe steatosis (χ2=51.46, P < 0.001), bridging fibrosis and early liver cirrhosis (χ2=36.59, P < 0.001), or bridging necrosis and large-scale necrosis (χ2=37.28, P < 0.001). Light microscopy showed that group A had extensive ballooning degeneration of hepatocytes, a large number of lipid droplets (mainly macrovesicular lipid droplets), disordered arrangement of the liver plate, lymphocyte infiltration, and focal bridging fibrosis; group B mainly had spotted focal necrosis, periportal fibrosis, lipid droplets with various sizes, a small amount of neutrophil infiltration, and ballooning degeneration of some hepatocytes; group C had ballooning degeneration of a small number of hepatocytes, focal perisinusoidal fibrosis, a small number of lesions with spotted focal necrosis, and a small number of lipid droplets in the cytoplasm of hepatocytes. Conclusion The degree of liver injury and fibrosis increases with the reduction in vitamin D level, and vitamin D measurement helps to evaluate the progression of NASH. -
Key words:
- Non-alcoholic Fatty Liver Disease /
- Vitamin D /
- FIB-4 Index /
- Interleukins
-
随着生活水平的提高与饮食习惯的改变,非酒精性脂肪性肝病(NAFLD)流行率逐渐上升,已成为世界上最常见的慢性肝病之一,在亚洲国家患病率约为25%[1],而在我国成年人中,患病率达29.2%[2]。NAFLD是一种与胰岛素功能障碍、遗传密切相关的代谢性肝损伤,是排除了酒精,由已知的其他肝损伤因素引发的肝细胞内脂质过度沉积所导致的肝脏疾病[3]。NAFLD不仅造成肝损伤,据研究[4],其对心脑血管、内分泌、泌尿系统亦产生影响,导致患者心脑血管疾病、2型糖尿病以及慢性肾病患病风险明显升高。
依据NAFLD严重程度,可分为非酒精性单纯性脂肪肝、非酒精性脂肪性肝炎(NASH)、肝硬化及肝细胞癌[5]。非酒精性单纯性脂肪肝通常被视为良性非进展性疾病,而NASH可逐渐发展至肝纤维化、肝硬化乃至肝细胞癌,故而NASH逐渐成为近年来研究的热点和难点。
维生素D起初因调节钙磷代谢而被人们熟知,之后有大量研究[6-7]发现其能够通过调节不同基因的表达而调控细胞增殖与分化,维生素D缺乏不仅导致骨骼相关疾病,而且影响着代谢综合征、内分泌系统疾病事件的发生。有研究[8]指出,维生素D水平与肝细胞脂质沉积、肝细胞坏死、肝纤维化程度密切相关。但也有学者[9]提出了不同观点,认为维生素D缺乏反而挽救了高脂膳食诱导的肝脏脂肪积累及脂肪酸代谢关键基因的转录。脂肪组织的内分泌功能十分活跃,能够分泌IL-18等细胞因子,IL-18依靠强大的生物活性能够直接损害肝细胞,在NASH中逐渐被人们重视[10];而IL-37作为近年新发现的抗炎因子在维持免疫平衡中发挥重要作用。ALT、TBil、TC、TG已被证实为脂肪性肝病发生的独立影响因素[11],因此,本研究通过比较不同1, 25(OH)2D3水平下NASH患者ALT、AST、TBil、TC、TG水平及FIB-4指数、肝脏病理分级以阐明维生素D缺乏与肝纤维化及病情严重程度之间的关系,并检测IL-18、IL-37水平以探究NASH可能的发生机制,为防治NASH提供更多参考。
1. 资料与方法
1.1 研究对象
选取2020年1月—2021年10月冬春季在本院感染科住院治疗的NASH患者。纳入标准:(1)年龄18~60岁,无饮酒史;(2)符合《非酒精性脂肪性肝病防治指南(2018年更新版)》[12]诊断标准;(3)临床资料、数据完善无缺失。排除标准:(1)病毒性肝炎、酒精性肝炎、自身免疫性肝炎、药物性肝炎、肝豆状核变性等其他原因导致肝损伤者;(2)使用激素或免疫抑制剂;(3)合并恶性肿瘤、甲状腺疾病、肾病、炎症性肠病、库欣综合征等导致脂肪肝的特殊情况。
1.2 研究方法
1.2.1 观察指标
入组时记录患者年龄、性别,测定实验室指标包括1, 25(OH)2D3、ALT、AST、TBil、TC、TG、IL-18、IL-37、PLT。
1.2.2 研究方法
所有受试者在入组时抽取5 mL空腹静脉血,以3000 r/min离心5 min,收集血清,储存在EDTA试管中。通过串联质谱法进行1, 25(OH)2D3定性和定量检测[美国AB公司液相色谱串联质谱仪(API400)]。使用全自动生化分析仪(美国BECKMAN公司)检测血清ALT、AST、TBil水平。采用ELISA法检测血清TC、TG、IL-18、IL-37水平(美国PD公司),使用美国Thermo公司生产的MK3酶标仪测定450 nm处的A值。采用血细胞计数仪测量PLT水平。
1.2.3 分组
美国国家科学院医学研究所定义血清1, 25(OH)2D3缺乏的标准为<20 ng/mL,不足为20~ 30 ng/mL,充足为>30 ng/mL[13]。根据血清1, 25(OH)2D3水平将受试者分为3组:A组为1, 25(OH)2D3缺乏组(<20 ng/mL);B组为1, 25(OH)2D3不足组(20~30 ng/mL);C组为1, 25(OH)2D3充足组(>30 ng/mL)。
1.2.4 FIB-4指数计算
FIB-4=年龄(岁)×AST(U/L)/[PLT(109/L)×ALT(U/L)1/2]
1.2.5 肝组织活检
在B超引导下,使用沪产160 mm× 16G穿刺针,在患者呼气末屏住呼吸时负压吸取长度超过1 cm的肝组织,经10%中性甲醛固定、石蜡包埋,切片为5 μm后行HE染色,依据Kleiner等[14]及张荣春等[15]建议的肝脏病理分级标准进行分级。
1.3 统计学方法
使用SPSS 25.0统计软件分析数据。计量资料以x±s表示,多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。计数资料组间比较采用χ2检验。相关性采用Pearson相关分析。P<0.05为差异有统计学意义。
2. 结果
2.1 一般资料
共纳入NASH患者120例,其中男69例,女51例,平均年龄(39.71±10.49)岁。A、B、C 3组各40例,3组患者的年龄和性别比较差异均无统计学意义(P值均>0.05)(表 1)。
表 1 3组患者观察指标比较Table 1. Comparison of observation indexes of three groups指标 A组
(n=40)B组
(n=40)C组
(n=40)统计值 P值 男性[例(%)] 22(55.00) 21(52.50) 26(65.00) χ2=3.45 0.178 年龄(岁) 41.35±7.33 38.30±12.57 40.10±9.96 F=1.30 0.275 1, 25(OH)2D3(ng/mL) 17.98±1.60 24.92±1.811) 33.21±2.741)2) F=772.21 <0.001 ALT(U/L) 81.72±10.13 55.44±13.481) 33.45±8.551)2) F=333.35 <0.001 AST(U/L) 73.20±15.27 44.40±10.681) 27.70±6.721)2) F=323.76 <0.001 TBil(μmol/L) 19.84±3.26 14.10±4.691) 13.42±4.911) F=30.66 <0.001 FIB-4指数 3.42±1.31 2.38±1.081) 1.40±0.621)2) F=78.31 <0.001 TC(mmol/L) 6.67±2.11 5.69±1.041) 4.71±1.091)2) F=38.38 <0.001 TG(mmol/L) 3.61±1.51 2.89±0.991) 2.12±1.011)2) F=30.75 <0.001 IL-18(ng/mL) 200.90±26.38 167.55±31.811) 148.23±33.631)2) F=42.37 <0.001 IL-37(ng/mL) 17.97±3.81 20.10±4.361) 24.96±3.311)2) F=70.56 <0.001 注:与A组比较,1)P<0.05;与B组比较,2)P<0.05。 2.2 3组患者1, 25(OH)2D3水平及肝功能比较
结果显示,与A组比较,B、C两组患者1, 25(OH)2D3水平均显著升高(P值均<0.05),而ALT、AST、TBil水平均显著下降(P值均<0.05)。与B组比较,C组患者1, 25(OH)2D3水平升高,ALT、AST水平下降,差异均有统计学意义(P值均<0.05)(表 1)。
2.3 3组患者FIB-4指数及TC、TG、IL-18、IL-37水平比较
结果显示,与A组比较,B、C两组患者FIB-4指数和TC、TG、IL-18水平均明显降低(P值均<0.05),IL-37水平明显升高(P<0.05)。与B组比较,C组患者FIB-4指数和TC、TG、IL-18水平均降低,IL-37水平升高,差异均有统计学意义(P值均<0.05)(表 1)。
2.4 1, 25(OH)2D3与ALT、AST、TBil、TC、TG、IL-18、IL-37水平及FIB-4指数的相关性分析
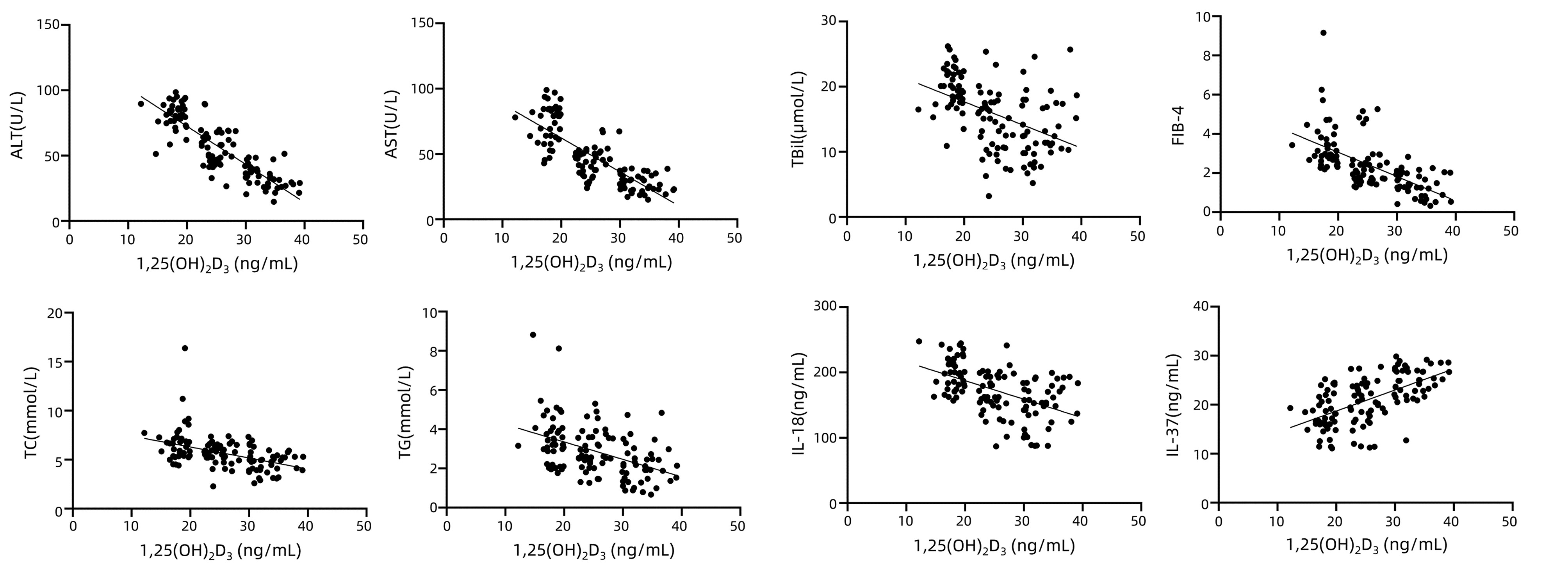
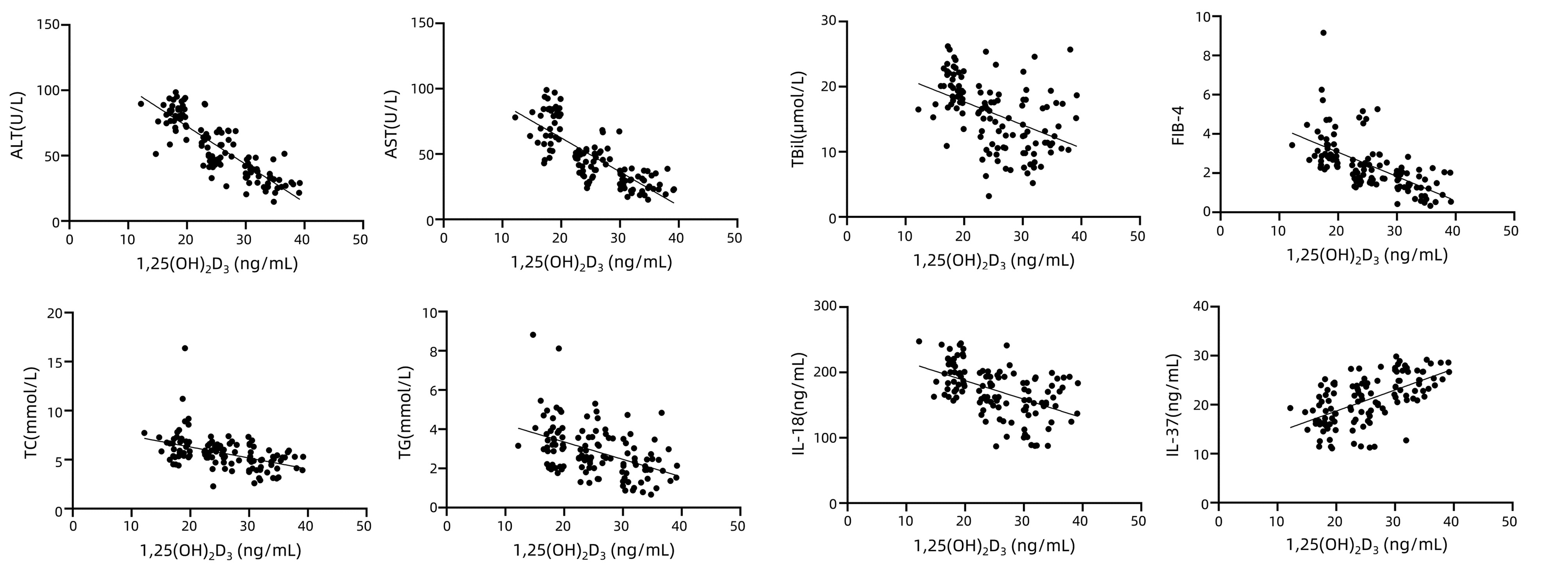
相关性分析结果显示,1, 25(OH)2D3与ALT(r=-0.84,P<0.001)、AST(r=-0.77,P<0.001)、TBil(r=-0.32,P<0.001)、TC(r=-0.45,P<0.001)、TG(r=-0.42,P<0.001)、IL-18(r=-0.40,P<0.001)及FIB-4指数(r=-0.62,P<0.001)均呈负相关,而与IL-37(r=0.59,P<0.001)呈正相关(图 1)。
2.5 3组患者肝脏病理组织学比较
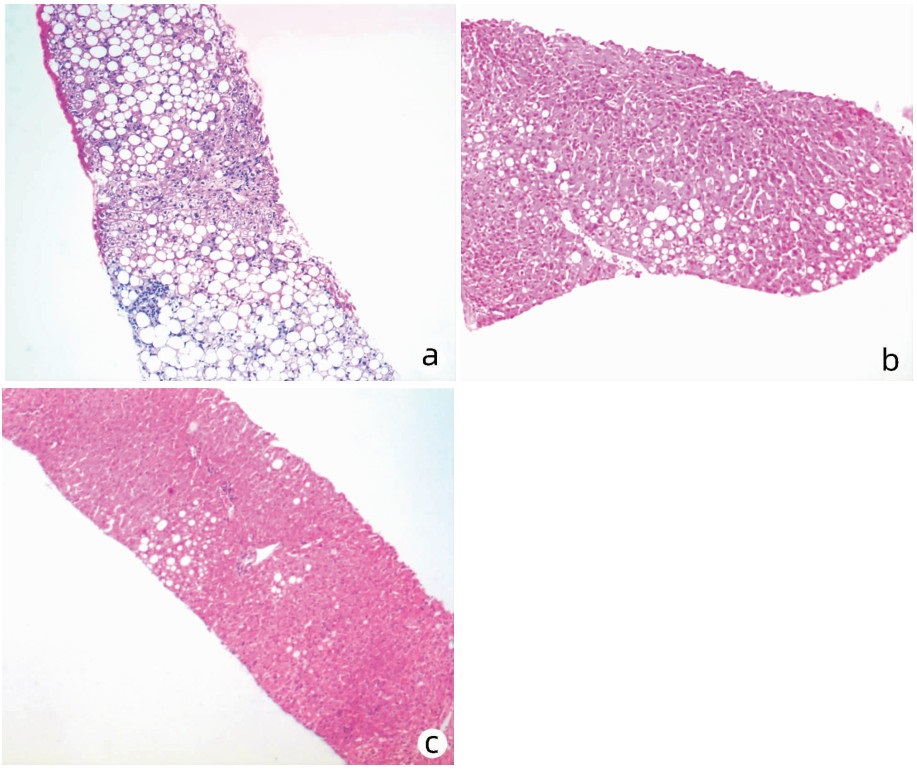
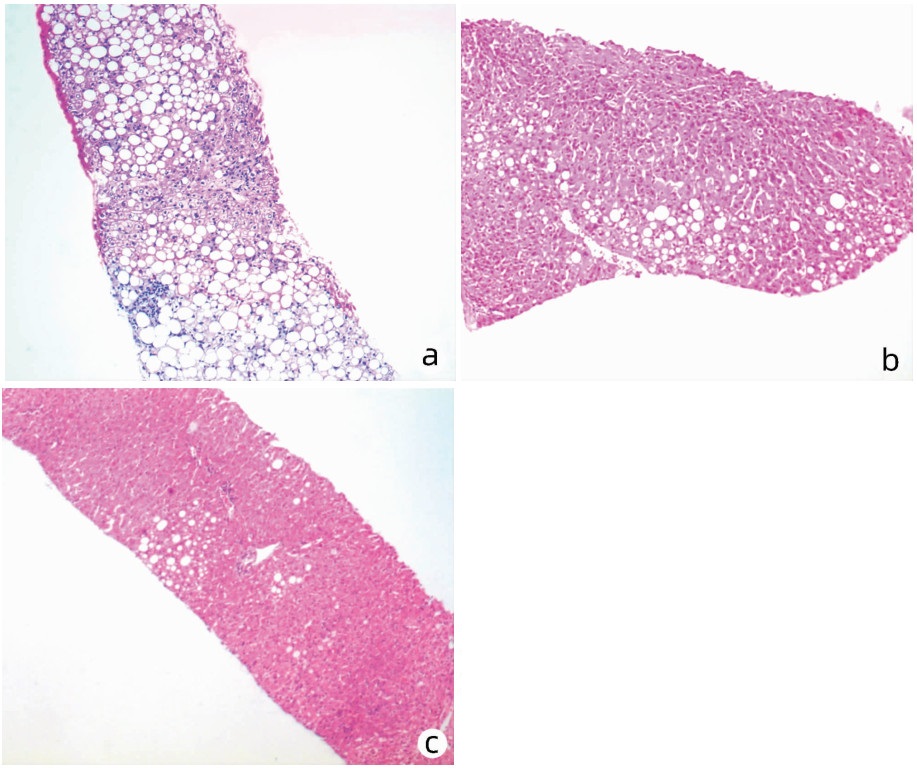
与A组相比,B、C组中与重度脂肪变、桥接纤维化与早期肝硬化、桥接坏死与大片坏死比例下降,且相较于B组,C组比例更低,差异均有统计学意义(P值均<0.05)(表 2)。光镜下可见A组患者肝细胞广泛气球样变,肝细胞胞质内出现大量大泡性为主的脂滴,肝板排列紊乱,大量淋巴细胞浸润,局灶桥接纤维化(图 2a);B组多数为点灶坏死,门静脉周围纤维化,脂滴大小不等,少量中性粒细胞浸润,部分肝细胞气球样变,肝小叶结构尚清晰(图 2b);C组少量肝细胞气球样变,局灶窦周纤维化,少数点灶坏死,肝细胞胞质可见少量脂滴,大多数为大泡性,部分为小泡性或混合性(图 2c)。
表 2 3组患者的肝脏病理组织学比较Table 2. Comparison of liver histopathology among the three groups肝脏病理组织学 A组
(n=40)B组
(n=40)C组
(n=40)χ2值 P值 脂肪变分级[例(%)] 51.46 <0.001 S0~S1 7(17.5) 27(67.5) 38(95.0) S2~S3 33(82.5) 13(32.5) 2(5.0) 肝纤维化分期[例(%)] 36.59 <0.001 F0~F2 14(35.0) 29(72.5) 39(97.5) F3~F4 26(65.0) 11(27.5) 1(2.5) 炎症分期[例(%)] 37.28 <0.001 H1~H2 6(15.0) 22(55.0) 32(80.0) H3~H4 34(85.0) 18(45.0) 8(20.0) 3. 讨论
在世界范围内,一般人群中NAFLD患病率可达20%~30%[16],其中NASH作为NAFLD的严重类型是心血管疾病的独立危险因素[17]。近年来,NASH发病率上升了5倍,且更多发生于年轻人,预测2030年德国NASH发病率将进一步增加15%[18],成为肝移植的最常见适应证。肝纤维化程度是反映NAFLD预后的主要标志[19],也可以用来区分非酒精性单纯性脂肪肝和NASH,因此肝纤维化检测在NASH患者中具有重要意义。已有FibroScan、FIB-4指数、APRI等无创方式来诊断及预测肝纤维化程度,但肥胖症严重影响了FibroScan的检测成功率,25%的患者无法获取准确的肝脏弹性值[20],而FIB-4指数因易获得,准确性与FibroScan相当,在几种无创纤维化检测方法中占据一定优势。目前,肝穿刺活检病理分级为评估脂肪变、纤维化及炎症程度的金标准,因此,本研究选取FIB-4指数及肝脏病理组织学作为评判肝纤维化程度的指标。
维生素D作为一种多效性激素除了参与钙稳态之外,也参与免疫炎症和代谢过程。已有研究[21-22]证实,维生素D缺乏与胰岛素抵抗相关疾病密不可分,如2型糖尿病、NAFLD及代谢综合征。在以往的研究中,学者们试图回答补充维生素D是否可以改善NAFLD,但结果存在争议。例如,Dabbaghmanesh等[23]对NAFLD患者及转氨酶正常的非糖尿病维生素D缺乏患者补充维生素D3(50 000 IU/周),结果发现与安慰剂相比,补充维生素D3未显著改变肝酶水平;Geier等[24]研究中NASH患者每日补充2100 IU维生素D3,48周后NASH患者的血清ALT水平显著降低。针对这一问题,本研究拟探讨维生素D水平与肝纤维化及病情严重程度之间的关系,为后期NASH治疗提供新的线索。
1, 25(OH)2D3是人体内维生素D的最终活性形式,其半衰期为2~3周,这些条件决定了1, 25(OH)2D3能够作为评估人体维生素D含量的相对稳定指标。对大部分人而言,获取维生素D的途径来源于阳光照射,已有众多研究[25-26]表明,适当的日照能够改善维生素D缺乏性佝偻病、骨质疏松等,而维生素D的生成量与日照中紫外线照射时长及强度密切相关,夏季和秋季相对日照时间较长、强度较大,为避免日照时长和强度对1, 25(OH)2D3水平的影响,本试验选择冬春季的住院患者为研究对象,提高结果的准确性。本研究结果显示,1, 25(OH)2D3水平越低,ALT、AST、TBil、TC、TG水平及FIB-4指数越高,肝细胞损伤范围越大,胞质内脂肪沉积越多,表明维生素D缺乏的NASH患者肝损伤、肝纤维化程度更明显,1, 25(OH)2D3水平可以在一定程度上反映病情进展情况,NASH患者补充维生素D可提高脂肪清除能力,减少脂质沉积,减轻肝损伤,减慢肝纤维化进程。
IL-18致使肝脏微循环受损,逐步加重肝细胞线粒体破环,导致肝细胞脂质摄取和肝细胞炎症因子的生成增加,亦可调节自然杀伤细胞分化,同时诱导多种多肽介质的产生,引起局部炎症反应,还能够刺激巨噬细胞生成一氧化氮,加强诱导型一氧化氮合酶的活性,诱导增强溶性细胞间黏附因子1的表达,促进肝细胞凋亡坏死[27]。IL-37降低肝细胞和Kupffer细胞产生的促炎细胞因子和趋化因子的能力,以及减少中性粒细胞激活和呼吸爆发,直接保护肝细胞免受氧化诱导的损伤[28]。本研究证实,随着1, 25(OH)2D3水平升高,肝损伤减轻,IL-18水平逐渐下降,而IL-37水平上升,提示NASH患者的肝纤维化及病情严重程度与IL-18高表达、IL-37低表达有关,炎症反应及氧化应激促进了肝损伤的进展,通过补充维生素D可能减轻炎症反应及氧化应激。
综上所述,维生素D水平与NASH患者肝纤维化及病情严重程度密切相关,可以作为评估肝损伤程度的重要指标,同时为干预NASH提供新的方向,适时补充维生素D有望减轻肝损伤,减慢肝纤维化进程,但合适的补充剂量、时间及疗程还有待进一步探讨。
-
表 1 3组患者观察指标比较
Table 1. Comparison of observation indexes of three groups
指标 A组
(n=40)B组
(n=40)C组
(n=40)统计值 P值 男性[例(%)] 22(55.00) 21(52.50) 26(65.00) χ2=3.45 0.178 年龄(岁) 41.35±7.33 38.30±12.57 40.10±9.96 F=1.30 0.275 1, 25(OH)2D3(ng/mL) 17.98±1.60 24.92±1.811) 33.21±2.741)2) F=772.21 <0.001 ALT(U/L) 81.72±10.13 55.44±13.481) 33.45±8.551)2) F=333.35 <0.001 AST(U/L) 73.20±15.27 44.40±10.681) 27.70±6.721)2) F=323.76 <0.001 TBil(μmol/L) 19.84±3.26 14.10±4.691) 13.42±4.911) F=30.66 <0.001 FIB-4指数 3.42±1.31 2.38±1.081) 1.40±0.621)2) F=78.31 <0.001 TC(mmol/L) 6.67±2.11 5.69±1.041) 4.71±1.091)2) F=38.38 <0.001 TG(mmol/L) 3.61±1.51 2.89±0.991) 2.12±1.011)2) F=30.75 <0.001 IL-18(ng/mL) 200.90±26.38 167.55±31.811) 148.23±33.631)2) F=42.37 <0.001 IL-37(ng/mL) 17.97±3.81 20.10±4.361) 24.96±3.311)2) F=70.56 <0.001 注:与A组比较,1)P<0.05;与B组比较,2)P<0.05。 表 2 3组患者的肝脏病理组织学比较
Table 2. Comparison of liver histopathology among the three groups
肝脏病理组织学 A组
(n=40)B组
(n=40)C组
(n=40)χ2值 P值 脂肪变分级[例(%)] 51.46 <0.001 S0~S1 7(17.5) 27(67.5) 38(95.0) S2~S3 33(82.5) 13(32.5) 2(5.0) 肝纤维化分期[例(%)] 36.59 <0.001 F0~F2 14(35.0) 29(72.5) 39(97.5) F3~F4 26(65.0) 11(27.5) 1(2.5) 炎症分期[例(%)] 37.28 <0.001 H1~H2 6(15.0) 22(55.0) 32(80.0) H3~H4 34(85.0) 18(45.0) 8(20.0) -
[1] YOUNOSSI Z, ANSTEE QM, MARIETTI M, et al. Global burden of NAFLD and NASH: Trends, predictions, risk factors and prevention[J]. Nat Rev Gastroenterol Hepatol, 2018, 15(1): 11-20. DOI: 10.1038/nrgastro.2017.109. [2] ESTES C, ANSTEE QM, ARIAS-LOSTE MT, et al. Modeling NAFLD disease burden in China, France, Germany, Italy, Japan, Spain, United Kingdom, and United States for the period 2016-2030[J]. J Hepatol, 2018, 69(4): 896-904. DOI: 10.1016/j.jhep.2018.05.036. [3] WATT MJ, MIOTTO PM, de NARDO W, et al. The liver as an endocrine organ-linking NAFLD and insulin resistance[J]. Endocr Rev, 2019, 40(5): 1367-1393. DOI: 10.1210/er.2019-00034. [4] TILG H, MOSCHEN AR, RODEN M. NAFLD and diabetes mellitus[J]. Nat Rev Gastroenterol Hepatol, 2017, 14(1): 32-42. DOI: 10.1038/nrgastro.2016.147. [5] SANTHEKADUR PK, KUMAR DP, SANYAL AJ. Preclinical models of non-alcoholic fatty liver disease[J]. J Hepatol, 2018, 68(2): 230-237. DOI: 10.1016/j.jhep.2017.10.031. [6] GIL Á, PLAZA-DIAZ J, MESA MD. Vitamin D: Classic and novel actions[J]. Ann Nutr Metab, 2018, 72(2): 87-95. DOI: 10.1159/000486536. [7] CIEBIERA M, WŁODARCZYK M, CIEBIERA M, et al. Vitamin D and uterine fibroids-review of the literature and novel concepts[J]. Int J Mol Sci, 2018, 19(7): 2051. DOI: 10.3390/ijms19072051. [8] MARADANA MR, YEKOLLU SK, ZENG B, et al. Immunomodulatory liposomes targeting liver macrophages arrest progression of nonalcoholic steatohepatitis[J]. Metabolism, 2018, 78: 80-94. DOI: 10.1016/j.metabol.2017.09.002. [9] LIU XJ, WANG BW, ZHANG C, et al. Vitamin D deficiency attenuates high-fat diet-induced hyperinsulinemia and hepatic lipid accumulation in male mice[J]. Endocrinology, 2015, 156(6): 2103-2113. DOI: 10.1210/en.2014-2037. [10] ZHAN ZM, JIANG YQ, HU ZJ, et al. Relationship between serum IL-18 expression level and liver injury in children with fatty liver[J]. Exp Lab Med, 2017, 35(2): 274-275, 283. DOI: 10.3969/j.issn.1674-1129.2017.02.047.詹忠明, 江永青, 胡志坚, 等. 儿童脂肪肝患者血清IL-18表达水平与肝损伤的关系[J]. 实验与检验医学, 2017, 35(2): 274-275, 283. DOI: 10.3969/j.issn.1674-1129.2017.02.047. [11] DENG J, ZHANG YH, DANG SS, et al. The change in the prevalence of fatty liver disease and related influencing factors among Karamay residents in 2009-2016 and related influencing factors[J]. J Clin Hepatol, 2021, 37(7): 1609-1613. DOI: 10.3969/j.issn.1001-5256.2021.07.026.邓江, 张永红, 党双锁, 等. 克拉玛依市居民2009年-2016年脂肪性肝病患病率变化及影响因素分析[J]. 临床肝胆病杂志, 2021, 37(7): 1609-1613. DOI: 10.3969/j.issn.1001-5256.2021.07.026. [12] National Workshop on Fatty Liver and Alcoholic Liver Disease, Chinese Society of Hepatology, Chinese Medical Association; Fatty Liver Expert Committee, Chinese Medical Doctor Association. Guidelines of prevention and treatment for nonalcoholic fatty liver disease: A 2018 update[J]. J Clin Hepatol, 2018, 34(5): 947-957. DOI: 10.3969/j.issn.1001-5256.2018.05.007.中华医学会肝病学分会脂肪肝和酒精性肝病学组, 中国医师协会脂肪性肝病专家委员会. 非酒精性脂肪性肝病防治指南(2018年更新版)[J]. 临床肝胆病杂志, 2018, 34(5): 947-957. DOI: 10.3969/j.issn.1001-5256.2018.05.007. [13] PLUDOWSKI P, HOLICK MF, GRANT WB, et al. Vitamin D supplementation guidelines[J]. J Steroid Biochem Mol Biol, 2018, 175: 125-135. DOI: 10.1016/j.jsbmb.2017.01.021. [14] KLEINER DE, BRUNT EM. Nonalcoholic fatty liver disease: Pathologic patterns and biopsy evaluation in clinical research[J]. Semin Liver Dis, 2012, 32(1): 3-13. DOI: 10.1055/s-0032-1306421. [15] ZHANG RC, WANG AZ. Experience in the application of diagnostic criteria for nonalcoholic fatty liver (Draft) (With pathological analysis of 30 cases)[J]. Mod Pract Med, 2002, 14(12): 657-658. DOI: 10.3969/j.issn.1671-0800.2002.12.015.张荣春, 王爱忠. 《非酒精性脂肪肝诊断标准(草案)》应用的体会(附30例病理分析)[J]. 现代实用医学, 2002, 14(12): 657-658. DOI: 10.3969/j.issn.1671-0800.2002.12.015. [16] SIVELL C. Nonalcoholic fatty liver disease: A silent epidemic[J]. Gastroenterol Nurs, 2019, 42(5): 428-434. DOI: 10.1097/SGA.0000000000000443. [17] CHAKRAVARTHY MV, WADDELL T, BANERJEE R, et al. Nutrition and nonalcoholic fatty liver disease: Current perspectives[J]. Gastroenterol Clin North Am, 2020, 49(1): 63-94. DOI: 10.1016/j.gtc.2019.09.003. [18] YOUNOSSI Z, TACKE F, ARRESE M, et al. Global perspectives on nonalcoholic fatty liver disease and nonalcoholic steatohepatitis[J]. Hepatology, 2019, 69(6): 2672-2682. DOI: 10.1002/hep.30251. [19] YEO SC, ONG WM, CHENG K, et al. Weight loss after bariatric surgery predicts an improvement in the non-alcoholic fatty liver disease (NAFLD) fibrosis score[J]. Obes Surg, 2019, 29(4): 1295-1300. DOI: 10.1007/s11695-018-03676-5. [20] WONG GL. Update of liver fibrosis and steatosis with transient elastography (Fibroscan)[J]. Gastroenterol Rep (Oxf), 2013, 1(1): 19-26. DOI: 10.1093/gastro/got007. [21] SACERDOTE A, DAVE P, LOKSHIN V, et al. Type 2 diabetes mellitus, insulin resistance, and vitamin D[J]. Curr Diab Rep, 2019, 19(10): 101. DOI: 10.1007/s11892-019-1201-y. [22] HU TP, TANG SD, YU ZB. Relationship between Vitamin D level in children and adolescents with nonalcoholic fatty liver disease: A Meta-analysis[J]. J Clin Hepatol, 2021, 37(3): 627-631. DOI: 10.3969/j.issn.1001-5256.2021.03.024.胡庭鹏, 唐苏丹, 余泽波. 儿童和青少年非酒精性脂肪性肝病与维生素D水平关系的Meta分析[J]. 临床肝胆病杂志, 2021, 37(3): 627-631. DOI: 10.3969/j.issn.1001-5256.2021.03.024. [23] DABBAGHMANESH MH, DANAFAR F, ESHRAGHIAN A, et al. Vitamin D supplementation for the treatment of non-alcoholic fatty liver disease: A randomized double blind placebo controlled trial[J]. Diabetes Metab Syndr, 2018, 12(4): 513-517. DOI: 10.1016/j.dsx.2018.03.006. [24] GEIER A, EICHINGER M, STIRNIMANN G, et al. Treatment of non-alcoholic steatohepatitis patients with vitamin D: A double-blinded, randomized, placebo-controlled pilot study[J]. Scand J Gastroenterol, 2018, 53(9): 1114-1120. DOI: 10.1080/00365521.2018.1501091. [25] MARWAHA RK, YENAMANDRA VK, SREENIVAS V, et al. Regional and seasonal variations in ultraviolet B irradiation and vitamin D synthesis in India[J]. Osteoporos Int, 2016, 27(4): 1611-1617. DOI: 10.1007/s00198-015-3427-0. [26] SERRANO MA, CAÑADA J, MORENO JC, et al. Solar ultraviolet doses and vitamin D in a northern mid-latitude[J]. Sci Total Environ, 2017, 574: 744-750. DOI: 10.1016/j.scitotenv.2016.09.102. [27] HARRISON SA, GOODMAN Z, JABBAR A, et al. A randomized, placebo-controlled trial of emricasan in patients with NASH and F1-F3 fibrosis[J]. J Hepatol, 2020, 72(5): 816-827. DOI: 10.1016/j.jhep.2019.11.024. [28] SAKAI N, van SWERINGEN HL, BELIZAIRE RM, et al. Interleukin-37 reduces liver inflammatory injury via effects on hepatocytes and non-parenchymal cells[J]. J Gastroenterol Hepatol, 2012, 27(10): 1609-1616. DOI: 10.1111/j.1440-1746.2012.07187.x. 期刊类型引用(6)
1. 陆悌明,任玲,张少轲. 纤维化指标与急性缺血性脑卒中患者血管内治疗后症状性颅内出血风险的相关性. 中国实用神经疾病杂志. 2024(03): 288-293 .  百度学术
百度学术2. 郭馨远,韩梅,马邓荣,昝晓晖,赵阳婷,吕小羽,李凯,陈重阳,王亚雯,刘靖芳. 2型糖尿病患者非酒精性脂肪肝及肝纤维化与骨骼肌质量关系的研究. 中华内分泌代谢杂志. 2024(08): 660-668 .  百度学术
百度学术3. 陈光耀,高晓,马英杰. 乙肝肝硬化患者维生素D水平与小肠细菌过度生长关系及与TLR4表达的相关性. 胃肠病学和肝病学杂志. 2024(10): 1299-1302 .  百度学术
百度学术4. 胡世杰,李栋,郭莉君,张敏,郭薇,张静. 维生素A、D水平与早产儿呼吸道感染肺炎后反复呼吸道感染相关性. 临床军医杂志. 2023(01): 92-94+99 .  百度学术
百度学术5. 李文豪,刘志平,赵致维,张金华. 25-羟维生素D、铁蛋白与代谢相关脂肪性肝病及FIB-4指数的相关性分析. 临床肝胆病杂志. 2023(08): 1867-1873 .  本站查看
本站查看6. 陈丹妮,王世令,路红,郑亚,王玉平,任茜. 维生素D与代谢相关脂肪性肝病的关系及机制. 协和医学杂志. 2023(06): 1258-1265 .  百度学术
百度学术其他类型引用(5)
-




 PDF下载 ( 2576 KB)
PDF下载 ( 2576 KB)

 下载:
下载:


 下载:
下载:
 百度学术
百度学术